第三章:院內型肺炎
3-2 診斷措施(一)臨床、放射線、血液、尿液檢查
重點提要
院內型肺炎及呼吸器相關肺炎須考慮到住院病人的複雜性,高比例免疫低下宿主及高死亡率。即時的診斷和適切的抗微生物製劑,仍是治療成功的最重要關鍵。特別要關注的是,移植病人、腫瘤化療病人、長期使用類固醇等免疫不全宿主,易發生社區型肺炎少見的黴菌及病毒的感染。在診斷上,電腦斷層較胸部 X 片能提高診斷敏感度及特異性,血液培養敏感度不高,但有助於診斷肺外散布型感染。生物標記及肺部感染指標雖然仍無法成為診斷及調整抗生素的單一指標,但生物標記在早期診斷黴菌感染上有重要的角色。尿液抗原檢測提供快速檢測退伍軍人症的方法,但要注意其敏感度較低的問題。而分子生物學的檢查,提供了診斷肺囊蟲肺炎及病毒性肺炎的較敏感檢驗方法。呼吸器相關事件的偵測,雖嘗試增加了自動化進行呼吸器相關肺炎的概念,但尚無法達到理想的敏感度及特異度,仍不建議以呼吸器相關事件的偵測來協助呼吸器相關肺炎之診斷。
主編:簡榮彥
副編:王振泰
一、臨床肺部感染指數(Clinical pulmonary infection score)之診斷價值
加入書籤
(一)臨床肺部感染指數(Clinical pulmonary infection score, CPIS)
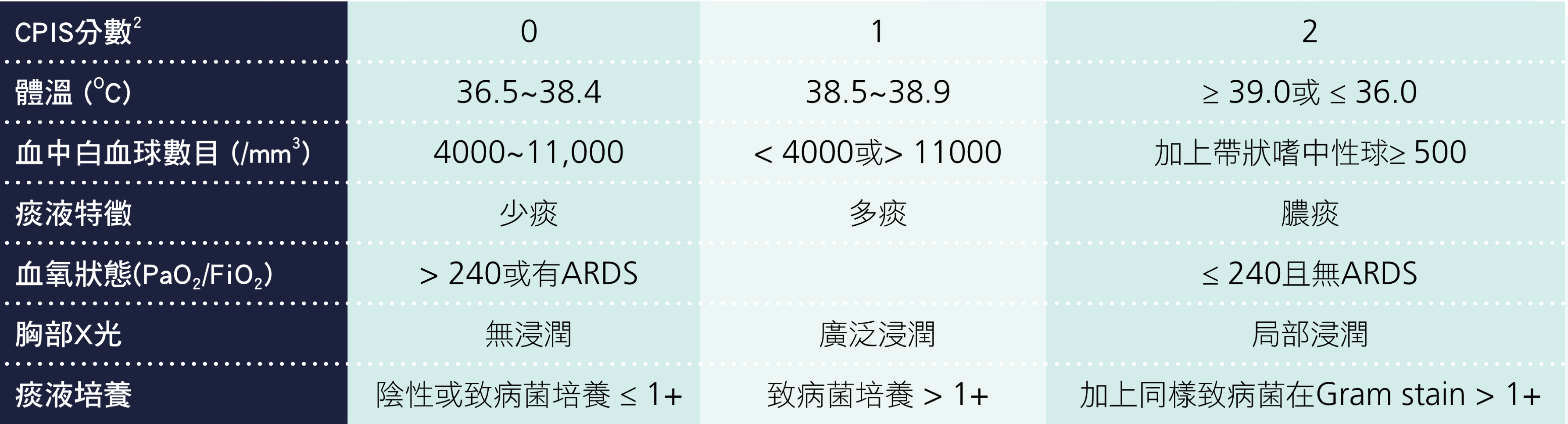
CPIS 最早由 Pugin 等人於 1990 年提出 [1],原本是用來預測呼吸器相關肺炎(Ventilator associated pneumonia, VAP)發生的可能性。其內容包含體溫、血中白血球數目、痰液特徵、血氧狀況、胸部 X 光及痰液培養等六項,每項分數則為 0 到 2 分(總分 0 到 12 分)。分數越高則嚴重度越高(參見表 3.2.1.)[2] 。Pugin發現 CPIS 大於 6 分的病人,確定為肺炎的敏感度(sensitivity)和特異性(specificity)分別為 93% 和 100%。不過後續的研究發現 CPIS 大於 6 分在診斷肺炎的可信度並不如原先預期 [3]。
表 3.2.1 臨床肺部感染指數(Clinical pulmonary infection score, CPIS)
(二)本節重要臨床問題
對於臨床懷疑 HAP/VAP 的病人,CPIS 是否可以當作常規診斷工具?
在 2011 的一篇統合分析(meta-analysis),CPIS 在 VAP 診斷的敏感性和特異性分別為 65%(95% 信賴區間(confidence interval, CI): 61~69%)和 64%(95% CI: 60∼67%)[4]。因此,CPIS 並不建議常規用於 HAP/VAP 診斷上 [2][5][6]。對於已診斷 HAP/VAP 的病人,CPIS 是否可以作為監測的工具?
有些較早期研究指出 CPIS 可以做為使用抗生素長短之參考。藉由 CPIS 的每日評估,CPIS 可以用來預估病人預後,或決定使用較短程的抗生素 [7]。根據 2017 年的 meta-analysis,CPIS 在預測 VAP 病人死亡風險的曲線下方的面積(area under the curve, AUC)為 0.64(95% CI: 0.55-0.72)[8]。但近年來,並沒有較大規模的研究用 CPIS 去評估監測治療結果的效益。但 CPIS 的六個分項評估內容,也已包含在我們一般對於 HAP/VAP 病人的常規監測中 [9]。CPIS 或可成為評估 HAP/VAP 病人臨床監測預後以及停抗生素的其中一種指標工具 [6][9]。
| GRADE 建議等級 | 臨床建議內容 | 參考文獻 |
|---|---|---|
| 2C | 對於已診斷 HAP/VAP 的病人,建議 CPIS 可以作為臨床監測預後以及停抗生素的其中一種指標工具。 | [1][2][3][4][5][6][7][8][9] |
二、肺炎的影像診斷工具
加入書籤
胸部影像檢查是診斷肺炎的必要工具,依 2016 年版美國感染症醫學會和胸腔醫學會所共同擬定的「院內型肺炎及呼吸器相關肺炎處置指引」中所陳述的定義 [5],肺炎的操作型定義為:出現新的肺部浸潤,且合併有相對應的感染症狀。其中所謂的「出現新的肺部浸潤」,即需有胸部影像檢查的結果來做為判斷,而「胸部X光」為目前最主要的肺炎影像檢查工具。
「胸部電腦斷層」可提供比胸部 X 光更詳細的肺實質及呼吸道解剖影像,新式胸部電腦斷層檢查由於在軟體及硬體上的長足進步,能顯著降低取像時間及輻射暴露劑量 [10]。目前已有臨床研究,欲評估及比較胸部電腦斷層和胸部 X 光,在肺炎診斷上的優劣。
(一)本節重要臨床問題
在「院內型肺炎」及「呼吸器相關肺炎」的診斷上,「胸部電腦斷層」相對於「胸部X光」,能提供更好的肺炎診斷率。
文獻回顧發現,過去研究對於胸部電腦斷層和胸部X光在肺炎診斷的比較,主要是針對「社區型肺炎」(community acquired pneumonia)的情境,針對院內型肺炎及呼吸器相關肺炎病人族群的文獻極少。而過去的研究對於這兩種影像診斷工具的比較,主要是評估兩者對於判斷「有無肺部浸潤」及「肺部浸潤型 態」時的差異,前者與診斷肺炎的靈敏度及特異度有關,後者與肺炎致病病原體的鑑別診斷有關。因電腦斷層可以更詳細的顯示肺實質變化,所以在判斷有無肺部浸潤以建立肺炎診斷方面,有著顯著的優勢。大部分的研究結果顯示,胸部電腦斷層比胸部X光,有更高的肺浸潤診斷靈敏度 [11][12][13][14]。在一近期發表的前瞻性社區型肺炎研究中 [11],若常規的對臨床上疑似為肺炎的病人執行胸部電腦斷層檢查,會大幅改變原本依胸部X光所做的判斷,且會改變醫師對病人的處置方式,在這個研究中,有 33% 原本在胸部X光上判斷為沒有肺浸潤的個案,因接受胸部電腦斷層而發現有肺浸潤。
在疑似「院內型肺炎」或「呼吸器相關肺炎」的病人身上,沒有證據可以支持例行性的執行胸部電腦斷層檢查能改善病人的死亡率或其他重要預後指標。
經文獻回顧,目前並無相關之研究結果可供參考。但有研究顯示,胸部電腦斷層比起胸部X光,有較好的肺炎嚴重度及預後的相關性 [15]。此外,胸部電腦斷層能提供詳細的肺實質變化評估,對於黴菌、病毒、或其它非典型細菌病原體所引發之肺炎,常需依賴胸部電腦斷層來做鑑別診斷。目前電腦斷層已廣泛運用於免疫功能不全、血液腫瘤、及移植等特殊病人族群的肺炎致病病原體之鑑別診斷 [16][17][18][19]。由社區型肺炎研究的資料看來,胸部電腦斷層相較於胸部 X 光,可以提供較好的肺炎診斷率,其結果應可外推至院內型肺炎及呼吸器相關肺炎族群。此外,胸部電腦斷層可以提供較好的肺實質變化的型態評估,有利於醫師對於肺炎致病病原體的鑑別診斷,在免疫功能不全、血液腫瘤、及移植等特殊病人族群有其重要性。現今的胸部電腦斷層技術,雖已降低輻射暴露劑量及縮短取像時間,但檢查相關風險仍顯著高於胸部 X 光,其中亦包括病人運送及檢查過程中之風險,這在生命跡象不穩定或呼吸器使用的病人中,尤其必須特別考量。
| GRADE 建議等級 | 臨床建議內容 | 參考文獻 |
|---|---|---|
| 2C | 相較於傳統的胸部 X 光,胸部電腦斷層可以增加肺炎的診斷率,以及幫助肺炎致病病原體的鑑別診斷。建議視病人之共病症及臨床狀況,來決定是否執行胸部電腦斷層檢查。 | [11][12][13][14][19] |
三、血液培養
加入書籤
針對感染的病人,在給予抗生素治療之前進行血液培養是目前普遍的常規作法。過去的研究發現,院內型肺炎(HAP)及呼吸器相關肺炎(VAP)病人血液培養陽性率不高 [20],但血液培養血液容易取得、操作簡單、便宜、特異性高,可能有助於診斷致病病原菌,診斷肺外感染及提供預後評估的參考。
(一)本節重要臨床問題
血液培養於診斷院內型肺炎致病病原菌的角色
文獻回顧發現,過去僅有一個研究針對血液培養對於診斷院內型肺炎致病病原菌進行評估。在一個前瞻性觀察研究中 [20],針對 162 名 VAP 病人進行研究,比較支氣管肺泡灌洗液(bronchial alveolar lavage(BAL)fluid)培養和 24 小時內血液培養的結果,發現血液培養陽性的比例僅為 16.7%,診斷致病菌的敏感度僅 26%,陽性預測率約 73%。另外,西班牙學者 [21]則發現,VAP 的菌血症,較常由抗甲氧苯青黴素金黃色葡萄球菌(methicillin-resistant Staphylococcus aureus, MRSA)所引起。血液培養有助於診斷肺外感染
雖然 VAP 病人血液培養陽性的比例僅為 16.7%,但在 22.2% 血液培養陽性的病人中,發現了肺部以外的感染 [20]。在外傷病人中 [22]也發現,血液培養陽性的 VAP 病人,較高比例(69% 比 38%)同時伴隨肺外感染。血液培養有助於提供疾病預後之參考
雖然上述研究結果血液培養陽性並不是 VAP 病人死亡的危險因子 [20],在一個單一中心回顧性的世代研究中 [21],發現在 199 個經微生物學證實的 VAP 事件中,其中 35 次(17.6%)伴隨有菌血症。雖然伴隨菌血症的 VAP 中,較高比例為過去曾經住院的病人、病人年紀亦較大(57.4 比 49.5 歲),但經過多變數分析後發現,伴隨菌血症的 VAP 病人,死亡率顯著較高(40.6% 比 19.3%, P = 0.02),是死亡的獨立危險因子,死亡風險為無菌血症病人的 2.86 倍(95% CI: 1.09 ~ 7.51)。在一個包括 9 個歐洲國家,27 個加護病房的多中心前瞻性研究 [23],分析 689 例使用侵入性呼吸器的插管病人後(224 例為 HAP,465 例為 VAP)發現,伴隨有菌血症的病人,死亡率顯著較高(57.1% 比 33%,P < 0.001),所需住院時間亦較長。在外傷病人也發現,血液培養陽性的 VAP 病人,需要使用較長時間的人工呼吸器(24 天 vs. 14 天, P < 0.05),需加護病房住院的時間較長(26 天 vs. 17 天, P < 0.05)及較長的住院時間(50 天 vs. 30 天, P < 0.05)。血液培養陽性亦和死亡率上升相關,但不是死亡的獨立危險因子 [22]。
雖然 HAP, VAP 病人血液培養的陽性率僅約 20%,仍有助於協助診斷致病病原菌。雖目前並無設計良好之大型研究支持進行血液培養有助於改善病人預後,但血液培養呈陽性是不良預後的重要危險因子,常伴隨抗藥性致病菌如金黃色葡萄球菌、鮑氏不動桿菌感染及肺外其他部位感染。因此,建議 HAP 及 VAP 病人宜例行作血液培養。
| GRADE 建議等級 | 臨床建議內容 | 參考文獻 |
|---|---|---|
| 1C | 對於院內型肺炎及呼吸器相關肺炎病人,建議例行作血液培養。 | [20][21][22][23] |
四、醫療照護相關黴菌性肺炎血液檢查的角色
加入書籤
黴菌性肺炎多發生在免疫力低下的病人,特別是在血液腫瘤科的病人 [24]。然而近幾年在加護病房除血液腫瘤病人外,當病人有大量類固醇的使用,慢性阻塞性肺病,肝硬化,器官移植,還有嚴重的流感等,偶而也會被診斷有黴菌性肺炎 [25]。最常見的黴菌性肺炎是 Aspergillus,然而黴菌性肺炎並不容易早期診斷。因此在許多白血病的治療指引中,建議當病人在化療後有嗜中性白血球低下的情形時,抽血檢驗麴菌(Aspergillus)細胞壁上的成分半乳甘露聚醣 galactomannan(GM),以早期診斷肺部麴菌症(pulmonary aspergillosis)[24]。相對的在非血液腫瘤的病人定期抽血檢驗 GM 的幫助仍有爭議 [24][25]。近幾年的文獻更建議使用支氣管肺泡灌洗液(BAL fluid)GM 的測定來診斷黴菌性肺炎,針對黴菌性肺炎 BAL 診斷的敏感度可以到達 88%,而血液檢驗的敏感度只有 40% [25]。聚合酶連鎖反應(Polymerase chain reaction,PCR)是近年來快速發展的領域,許多研究嘗試以血液檢體 PCR 的方式來協助黴菌性肺炎的診斷 [26],不過由於黴菌 DNA 抽取仍有不少困難,相對於 GM 的測定,目前運用 Aspergillus PCR 來診斷黴菌性肺炎的證據仍較為不足。
另一個可以在院內被診斷重要的黴菌性肺炎是肺囊蟲肺炎(Pneumocystis jirovecii pneumonia, PCP)[27]。以往 PCP 多診斷於人類免疫缺乏病毒(human immunodeficiency, HIV)感染的病人,但是近幾年在不少免疫力低下(癌症或是免疫療法)的病人於住院中也發現有 PCP 的肺炎。傳統上 PCP 在台灣多為臨床診斷,近幾年則有痰液檢體的免疫螢光染色或聚合酶連鎖反應可以幫助 PCP 的診斷 [28]。至於抽血檢驗,之前的 meta-analysis 統計 12 個研究發現 (1,3)-β-D-glucn 對肺囊蟲肺炎的敏感性為 96%(92~98%),特異性為 84%(83~86%)[29],因此在 2016 歐洲 PCP 的診斷指引中認為如果抽血檢驗 (1,3)-β-D-glucan 的結果是陰性的,可以排除 PCP 肺炎的可能性[30]。可惜的是在台灣有常規檢驗 (1,3)-β-D- glucan的 實驗室並不多。
五、病毒性肺炎血液檢查的角色
加入書籤
在院內型肺炎及呼吸器相關肺炎中,病毒感染多發生於免疫不全的病人;在免疫健全的病人族群,仍是以細菌為主要病原菌 [31]。但無論在免疫不全或免疫健全的病人族群中的病毒性院內型肺炎或呼吸器相關肺炎,皆是以巨細胞病毒(Cytomegalovirus,CMV)最為重要 [31]。 巨細胞病毒引起的肺炎比例,可能比我們想像的更高;在兩個小型的研究中,從急性呼吸窘迫症候群和免疫健全的呼吸器相關肺炎病人取得的肺部組織切片中,約有三成符合巨細胞病毒感染的病理變化 [32]。目前巨細胞病毒的檢測法,包括病毒培養,血中 pp65 抗原偵測,以及聚合酶連鎖反應(PCR)[33]。病毒培養敏感性低,且耗費時間;血中抗原偵測的敏感性 佳,而且可對病毒定量,但需要周邊血液檢體中有足夠量的白血球,而且較耗人力;聚合酶連鎖反應則具有高敏感性和低檢驗時間的優勢。但在評估是否確實為巨細胞病毒感染時,仍須謹慎評估檢驗的結果。若是單純以血中抗原偵測作為診斷的依據,可能約有 16% 的加護病房(intensive care unit, ICU)病人都有巨細胞病毒感染 [34]。但是,血清學偵測陽性和真正的巨細胞病毒感染並非同一件事,在不同的研究結論中 [35],都可以看到這個問題(血清學陽性:28~100% vs 巨細胞病毒感染:0~36%)。
另一個需要注意的病毒為流行性感冒病毒。流行性感冒病毒在流行季節時,也是屬於病毒性院內型肺炎的常見病原,尤其在 65 歲以上的老人、護理之家/慢性照護機構的住民、孕婦、慢性病共病、免疫不全以及肥胖的病人,致死性更高 [31]。目前診斷流行性感冒病毒感染的方法,包括病毒培養、免疫螢光法(immunofluorescence,IF)偵測病毒抗原、以及聚合酶連鎖反應 [36]。不過,以上三種檢驗方式,皆是以呼吸道檢體為檢驗檢體,而與傳統的鼻腔檢體相較,鼻咽處或支氣管肺泡灌洗液的檢體能提供較佳的診斷率 [36][37][38]。而美國藥物食品管理局目前核准的 28 種偵測流行性感冒病毒的聚合酶連鎖反應分析和其他分子檢驗,也 都是以呼吸道檢體,尤其是鼻咽拭子為檢驗對象 [39]。
(一)本節重要臨床問題:
- 在疑似巨細胞病毒感染的個案,建議以抽血檢驗的方式以協助診斷巨細胞病毒感染。
在目前現有的巨細胞病毒檢驗方式中,可以利用抽血方式檢驗的有病毒培養、血中抗原偵測,以及聚合酶連鎖反應(PCR)[33]。雖然血中抗原偵測及聚合酶連鎖反應都是相對高敏感性的檢查,但是,巨細胞病毒血清學偵測陽性和真正的巨細胞病毒感染並非同一件事。因此,如果要以抽血檢驗是否為巨細胞病毒感染,不建議以抽血檢驗結果單獨判斷,建議應與其他臨床資料一同審慎評估。
六、生物標記及尿液抗原
加入書籤
臨床上為了幫助診斷院內型肺炎(HAP)或呼吸器相關肺炎(VAP)而發展出一些檢驗工具,希望能找出某些體液中的分子,只有在體內呈現出發炎狀態特別是細菌感染時,存在著高濃度的變化,這就是所謂的生物標記,屬於體內蛋白質的一種,它們的存在跟疾病本身有關連性,使得它們可以成為有潛力的診斷工 具。理想上,這些生物標記的檢驗結果應該要比定量的細菌培養報告更早發出來。一種具備有高度敏感性的生物標記檢驗,能夠避免抗生素治療延遲,而有高度特異性的生物標記檢驗,也將能夠減少不必要的抗生素使用以及抗藥性的產生。目前臨床上常用的體液之生物標記檢驗包括了:前降鈣素(procalcitonin, PCT)、可溶性髓樣細胞誘導受體第一型(soluble triggering receptor expressed on myeloid cells, sTREM-1)以及 C-反應蛋白(C-reactive protein, CRP)。
PCT 是降鈣素的先驅物質,主要是由甲狀腺的 C 細胞和肺部的 K 細胞所分泌。當人體內受到內毒素的刺激時,全身的實質組織會快速的製造出 PCT。另外,雖然不常見但是 PCT 還是可能在無菌發炎或病毒感染狀態時表現出上升的結果。由於 PCT 本身在體內遭遇發炎反應有快速釋放以及較長半衰期的特性,使得它成為潛在有用的診斷工具 [40]。sTREM-1 是種醣蛋白屬於免疫球蛋白科的一員,已經被發現大量的表現在中性球及單核球,而這些細胞同時浸潤著被細菌或黴菌侵犯的組織 [41],所以被當作為微生物感染的生物指標來研究。另外,sTREM-1 也會透過 DNAX activation protein of 12kDa(DAP12)的訊號路徑啟動促炎媒介物的分泌,來放大發炎反應的表現。然而在最近幾個研究顯示 sTREM-1 在非感染引起的發炎變化也會上升,它在診斷感染症的角色顯得較不明確。CRP 是發炎反應的非特異性生物指標之一,主要在肝臟合成。當感染發生時,CRP 將快速產生,並且一旦刺激被移除時,CRP 將快速下降。不過在細菌感染、外傷、燙傷、外科手術及癌症狀態,CRP 也會急遽上升。血清中的 CRP 是個快速又非侵入性的生物標記,但是,只有有限的小型研究來檢視它能否成為呼吸器相關肺炎的指標 [40]。
尿液抗原診斷肺炎鏈球菌肺炎(pneumococcal urinary antigen test),作法簡便,報告時效快,約 15 分鐘,其敏感度約 50~80%,並有超過 90% 的特異性 [42];然而,如果病人在過去三個月內有發生過社區型肺炎,那麼此檢測將會呈現偽陽性的結果,亦即此尿液抗原陽性會持續一個月以上。另外在台灣所分離出的肺炎鏈球菌,對於 penicillin 以及第三代頭孢子素都有超過九成以上的感受性 [43]。因此對於一位疑似的 HAP/VAP 的病人檢測肺炎鏈球菌尿液抗原,若是其報告呈現為陽性,那麼經驗性使用的抗生素應該可以覆蓋到肺炎鏈球菌的範圍,就算是偽陽性也不會改變臨床預後,故此尿液抗原檢驗對 HAP/VAP 的個案之診斷幫助不大。
尿液抗原檢測退伍軍人症(Legionella urinary antigen test)的診斷陽性率約 80% [44],但目前市售的檢測試劑只能檢驗 Legionella pneumophila serogroup 1。根據美國疾病管制署(Centers for disease control and prevention, CDC)的建議,若是醫療機構發生以下任一事件,便要檢測尿液退伍軍人菌抗原以排除醫療照護相關肺炎的可能性,包括了在過去 12 個月有診斷出醫療照護相關退伍軍人症的個案,在過去兩個月環境中退伍軍人症的檢驗為陽性,近期因水品質的變化導致了退伍軍人菌的生長,如氯濃度下降。至於台灣 CDC 則建議,如果同一供水系統退伍軍人菌陽性樣本數達到 30% 以上,便要針對所有醫療照護相關肺炎感染病人常規執行尿液退伍軍人菌抗原檢驗。因此假如臨床上疑似 HAP/VAP 個案合併有上述情況,便要考慮此尿液抗原檢測。
(一)本節重要臨床問題
對於疑似 HAP/VAP 的病人,不建議使用 PCT 當作診斷工具來決定開始投予抗生素治療。
過去的研究及統合分析發現,PCT 作為診斷工具的敏感性和特異性大約分別為 67% 和 83%,並無法達到超過 90% 之敏感性和特異性。再者,一個近期的試驗把 ICU 的病人 [45],隨機分配到一組為標準照護,另一組以 PCT 為導向來決定抗生素的升階治療,目的是希望能增加早期適當抗生素使用來改善存活率,結果以 PCT 導向那組並沒有發現存活率的改善,反而引起了較多的呼吸器使用天數以及較長的 ICU 住院天數。故目前並不推薦使用 PCT 來診斷 HAP 或 VAP。對於疑似 HAP/VAP 的病人,不建議 CRP 當作診斷工具來決定開始投予抗生素治療。
過去少有研究針對 CRP 診斷呼吸器相關肺炎(VAP)的能力加以評估。一個觀察性的研究納入了 148 個接受呼吸器的病人,發現在診斷有肺炎的病人其 CRP 數據與沒有肺炎的病人一樣 [46];在一個納入了 28 位在院外心跳停止後回復了自發性的循環個案的研究中,CRP 的數據在有 VAP 和沒有 VAP 的病人中是一樣的 [47]。由於這些報告來自於觀察性研究,故其證據等級較低。另外這些研究都證實 CRP 無法確實的區分有 VAP 的個案及無 VAP 的個案。因此,CRP 的檢測可能會誤導臨床醫師的決策,而且使用 CRP 的數值來處置可能有 VAP 的病人所獲得的好處,也不 會比 CRP 的成本花費或檢驗負擔來的更高。所以臨床上並不推薦使用 CRP 來診斷 HAP/VAP 以及後續引導抗生素的治療。
七、呼吸器相關事件(Ventilator associated event)
加入書籤
(一)呼吸器相關事件(ventilator-associated event,VAE)及呼吸器相關性肺炎(ventilator-associated pneumonia,VAP)
呼吸器相關肺炎(VAP)指接受呼吸器治療 48 小時以上之病人併發肺炎感染,是院內感染重要的指標之一。但由於使用呼吸器病人的臨床狀況複雜,常常 很不容易清楚界定出病人是否有 VAP。有鑑於此,美國疾病管制署乃提出 VAE 的概念,希望藉由 VAE 監測所定義出的一連串流程,協助所謂 VAP 的指標監測。VAE 的監測定義,包含了眾多客觀、合理精簡的、可以自動化收集的、可能發生於使用呼吸器之成年病人的事證。主要包含了三個重要的結點:(1)使用呼吸的病人,在至少連續兩天的穩定期之後,發生了連續兩天持續惡化(氧氣需求增加)的狀況,此稱為 ventilator-associated condition(VAC);(2)在 VAC 的狀況中,有客觀證據顯示有發炎或感染的事實存在,此稱為 infection-related VAC(IVAC);(3)在 IVAC 確立的情形下,有陽性的實驗室或微生物學證據顯示有下呼吸道感染的狀況,此稱為 possible or probable VAP(VAE-VAP)。
(二)重要臨床問題
VAE 監測在偵察出 VAP 的角色
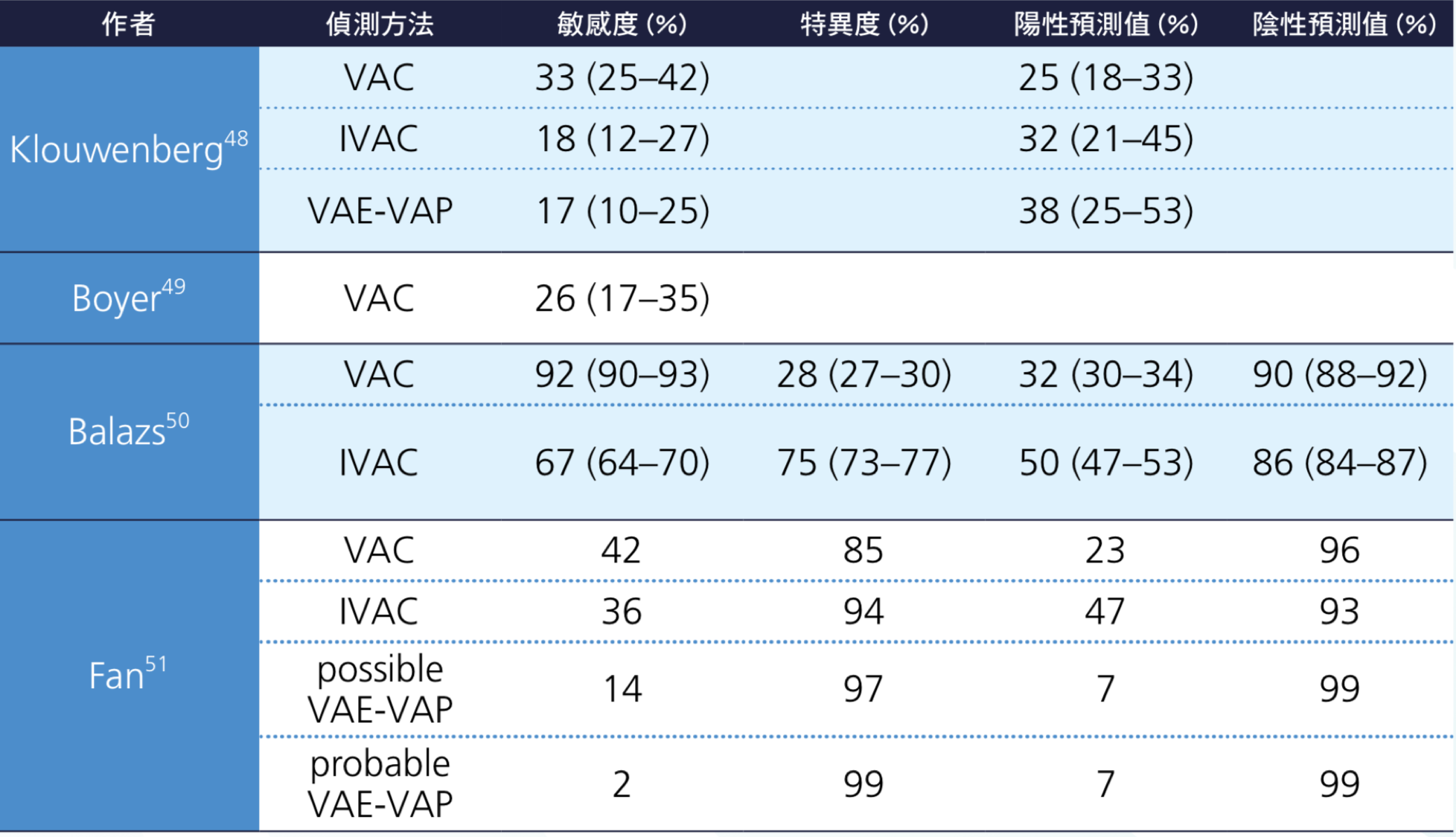
在 VAE 監測的定義擬定公佈之後,便有許多研究想要釐清,到底「VAE 監測與 VAP 的關連性」有多高?近年發表的文獻中指出以 VAC 偵測傳統 VAP 的敏感度有 25.9~92% [48][49][50],陽性預測能力(positive predictive value, PPV)有 25~32% [48][50],特異性有 28%,和陰性預測能力(negative predictive value, NPV)有 90% [50]。以 IVAC 來偵測傳統的 VAP,其敏感度有 18~67%,陽性預測率只有 32~ 50% [48][50],特異性為 75%,陰性預測率為 86% [50]。以 VAE-VAP 來偵測傳統的 VAP,其敏感度只有 17%(10~25%),陽性預測率只有 38%(25~53%)(參見表 3.2.2.)。
由上述這些指標性的文章可看到,以 VAE 來偵測傳統的 VAP,其效果在各個研究當中,其實並不一致。在 2016 年有一篇針對此議題的 meta-analysis [51],分析了 18 篇的研究報告指出,就偵測傳統 VAP 的 sensitivity 來說,VAC 是 41.8%, IVAC 是 36.3%,possible VAE-VAP 是 14.4%,probable VAE-VAP 是 1.6%;就偵測傳統 VAP 的 specificity 來說,VAC 是 84.5%,IVAC 是 94.0%,possible VAE-VAP 是 97.3%,probable VAE-VAP 是 99.3%;就偵測傳統 VAP 的陽性預測率來說,VAC 是 23.2%,IVAC 是 47.2%,possible VAE-VAP 是 7.4%, probable VAE-VAP 是 6.5%;就偵測傳統 VAP 的陰性預測率來說,VAC 是 95.6%,IVAC 是 93.3%,possible VAE-VAP 是 99.2%,probable VAE-VAP 是 99.1% [6]。由此可知,VAE 監測並不能精準的預測加護病房中傳統 VAP 的病人。其主要的原因在於,VAE 監測所規範的病人群,一開始便與傳統 VAP 的病人群不盡相同。
表 3.2.2 以 VAC, IVAC, VAE-VAP 來偵測傳統 VAP 的效能
| GRADE 建議等級 | 臨床建議內容 | 參考文獻 |
|---|---|---|
| 1A | VAE 監測並不能精準的預測加護病房中傳統 VAP 的病人,不建議以 VAE 監測來協助 VAP 之診斷。 | [48][49][50] |
八、參考文獻
加入書籤
Pugin J, Auckenthaler R, Mili N, et al. Diagnosis of ventilator-associated pneumonia by bacteriologic analysis of bronchoscopic and nonbronchoscopic "blind" bronchoalveolar lavage fluid. Am Rev Respir Dis 1991;143(5 Pt 1):1121-9. ↩︎ ↩︎
Zilberberg MD, Shorr AF. Ventilator-associated pneumonia: the clinical pulmonary infection score as a surrogate for diagnostics and outcome. Clin Infect Dis 2010;51 Suppl 1:S131-5. ↩︎ ↩︎ ↩︎
Fabregas N, Ewig S, Torres A, et al. Clinical diagnosis of ventilator associated pneumonia revisited: comparative validation using immediate post-mortem lung biopsies. Thorax 1999;54(10):867-73. ↩︎ ↩︎
Shan J, Chen HL, Zhu JH. Diagnostic accuracy of clinical pulmonary infection score for ventilator-associated pneumonia: a meta-analysis. Respir Care 2011;56(8):1087-94. ↩︎ ↩︎
Kalil AC, Metersky ML, Klompas M, et al. Management of Adults With Hospital-acquired and Ventilator-associated Pneumonia: 2016 Clinical Practice Guidelines by the Infectious Diseases Society of America and the American Thoracic Society. Clin Infect Dis 2016;63(5):e61-e111. ↩︎ ↩︎ ↩︎
Torres A, Niederman MS, Chastre J, et al. International ERS/ESICM/ESCMID/ALAT guidelines for the management of hospital-acquired pneumonia and ventilator-associated pneumonia. Eur Respir J 2017;50(3). ↩︎ ↩︎ ↩︎ ↩︎
Fartoukh M, Maitre B, Honore S, et al. Diagnosing pneumonia during mechanical ventilation: the clinical pulmonary infection score revisited. Am J Respir Crit Care Med 2003;168(2):173-9. ↩︎ ↩︎
Larsson J, Itenov TS, Bestle MH. Risk prediction models for mortality in patients with ventilator-associated pneumonia: A systematic review and meta-analysis. J Crit Care 2017;37:112-8. ↩︎ ↩︎
Bickenbach J, Marx G. Diagnosis of pneumonia in mechanically ventilated patients: what is the meaning of the CPIS? Minerva Anestesiol 2013;79(12):1406-14. ↩︎ ↩︎ ↩︎
Rubin GD. Computed tomography: revolutionizing the practice of medicine for 40 years. Radiology 2014;273(2 Suppl):S45-74. ↩︎
Claessens YE, Debray MP, Tubach F, et al. Early Chest Computed Tomography Scan to Assist Diagnosis and Guide Treatment Decision for Suspected Community-acquired Pneumonia. Am J Respir Crit Care Med 2015;192(8):974-82. ↩︎ ↩︎ ↩︎
Karhu JM, Ala-Kokko TI, Ahvenjarvi LK, et al. Early chest computed tomography in adult acute severe community-acquired pneumonia patients treated in the intensive care unit. Acta Anaesthesiol Scand 2016;60(8):1102-10. ↩︎ ↩︎
Self WH, Courtney DM, Mcnaughton CD, et al. High discordance of chest x-ray and computed tomography for detection of pulmonary opacities in ED patients: implications for diagnosing pneumonia. Am J Emerg Med 2013;31(2):401-5. ↩︎ ↩︎
Syrjala H, Broas M, Suramo I, et al. High-resolution computed tomography for the diagnosis of community-acquired pneumonia. Clin Infect Dis 1998;27(2):358-63. ↩︎ ↩︎
Haga T, Fukuoka M, Morita M, et al. Computed Tomography for the Diagnosis and Evaluation of the Severity of Community-acquired Pneumonia in the Elderly. Intern Med 2016;55(5):437-41. ↩︎
Patterson TF, Thompson GRR, Denning DW, et al. Executive Summary: Practice Guidelines for the Diagnosis and Management of Aspergillosis: 2016 Update by the Infectious Diseases Society of America. Clin Infect Dis 2016;63(4):433-42. ↩︎
Kupeli E, Eyuboglu FO, Haberal M. Pulmonary infections in transplant recipients. Curr Opin Pulm Med 2012;18(3):202-12. ↩︎
Kanne JP, Yandow DR, Meyer CA. Pneumocystis jiroveci pneumonia: high-resolution CT findings in patients with and without HIV infection. AJR Am J Roentgenol 2012;198(6):W555-61. ↩︎
Marom EM, Kontoyiannis DP. Imaging studies for diagnosing invasive fungal pneumonia in immunocompromised patients. Curr Opin Infect Dis 2011;24(4):309-14. ↩︎ ↩︎
Luna CM, Videla A, Mattera J, et al. Blood cultures have limited value in predicting severity of illness and as a diagnostic tool in ventilator-associated pneumonia. Chest 1999;116(4):1075-84. ↩︎ ↩︎ ↩︎ ↩︎ ↩︎
Agbaht K, Diaz E, Munoz E, et al. Bacteremia in patients with ventilator-associated pneumonia is associated with increased mortality: A study comparing bacteremic vs. nonbacteremic ventilator-associated pneumonia. Crit Care Med 2007;35(9):2064-70. ↩︎ ↩︎ ↩︎
Kunac A, Sifri ZC, Mohr AM, et al. Bacteremia and ventilator-associated pneumonia: a marker for contemporaneous extra-pulmonic infection. Surg Infect (Larchmt) 2014;15(2):77-83. ↩︎ ↩︎ ↩︎
Magret M, Lisboa T, Martin-Loeches I, et al. Bacteremia is an independent risk factor for mortality in nosocomial pneumonia: a prospective and observational multicenter study. Crit Care 2011;15(1):R62. ↩︎ ↩︎
Maschmeyer G, Carratala J, Buchheidt D, et al. Diagnosis and antimicrobial therapy of lung infiltrates in febrile neutropenic patients (allogeneic SCT excluded): updated guidelines of the Infectious Diseases Working Party (AGIHO) of the German Society of Hematology and Medical Oncology (DGHO). Ann Oncol 2015;26(1):21-33. ↩︎ ↩︎ ↩︎
Bassetti M, Bouza E. Invasive mould infections in the ICU setting: complexities and solutions. J Antimicrob Chemother 2017;72(Suppl 1):i39-i47. ↩︎ ↩︎ ↩︎
Morrissey CO, Chen SC, Sorrell TC, et al. Galactomannan and PCR versus culture and histology for directing use of antifungal treatment for invasive aspergillosis in high-risk haematology patients: a randomised controlled trial. Lancet Infect Dis 2013;13(6):519-28. ↩︎
Lu JJ, Lee CH. Pneumocystis pneumonia. J Formos Med Assoc 2008;107(11):830-42. ↩︎
Chien JY, Liu CJ, Chuang PC, et al. Evaluation of the automated Becton Dickinson MAX real-time PCR platform for detection of Pneumocystis jirovecii. Future Microbiol 2017;12:29-37. ↩︎
Onishi A, Sugiyama D, Kogata Y, et al. Diagnostic accuracy of serum 1,3-beta-D-glucan for pneumocystis jiroveci pneumonia, invasive candidiasis, and invasive aspergillosis: systematic review and meta-analysis. J Clin Microbiol 2012;50(1):7-15. ↩︎
Alanio A, Hauser PM, Lagrou K, et al. ECIL guidelines for the diagnosis of Pneumocystis jirovecii pneumonia in patients with haematological malignancies and stem cell transplant recipients. J Antimicrob Chemother 2016;71(9):2386-96. ↩︎
Chiche L, Forel JM, Papazian L. The role of viruses in nosocomial pneumonia. Curr Opin Infect Dis 2011;24(2):152-6. ↩︎ ↩︎ ↩︎
Papazian L, Doddoli C, Chetaille B, et al. A contributive result of open-lung biopsy improves survival in acute respiratory distress syndrome patients. Crit Care Med 2007;35(3):755-62. ↩︎
Boeckh M, Boivin G. Quantitation of cytomegalovirus: methodologic aspects and clinical applications. Clin Microbiol Rev 1998;11(3):533-54. ↩︎ ↩︎
Chiche L, Forel JM, Roch A, et al. Active cytomegalovirus infection is common in mechanically ventilated medical intensive care unit patients. Crit Care Med 2009;37(6):1850-7. ↩︎
Cohen JI. Cytomegalovirus in the intensive care unit: pathogen or passenger? Crit Care Med 2009;37(6):2095-6. ↩︎
Nguyen C, Kaku S, Tutera D, et al. Viral Respiratory Infections of Adults in the Intensive Care Unit. J Intensive Care Med 2016;31(7):427-41. ↩︎ ↩︎
Meerhoff TJ, Houben ML, Coenjaerts FE, et al. Detection of multiple respiratory pathogens during primary respiratory infection: nasal swab versus nasopharyngeal aspirate using real-time polymerase chain reaction. Eur J Clin Microbiol Infect Dis 2010;29(4):365-71. ↩︎
Sung RY, Chan PK, Choi KC, et al. Comparative study of nasopharyngeal aspirate and nasal swab specimens for diagnosis of acute viral respiratory infection. J Clin Microbiol 2008;46(9):3073-6. ↩︎
Centers for Disease Control and Prevention. Guidance for Clinicians on the Use of RT-PCR and Other Molecular Assays for Diagnosis of Influenza Virus Infection. Accessed Jan 29, 2018. ↩︎
Palazzo SJ, Simpson T, Schnapp L. Biomarkers for ventilator-associated pneumonia: review of the literature. Heart Lung 2011;40(4):293-8. ↩︎ ↩︎
Bouchon A, Dietrich J, Colonna M. Cutting edge: inflammatory responses can be triggered by TREM-1, a novel receptor expressed on neutrophils and monocytes. J Immunol 2000;164(10):4991-5. ↩︎
Mandell LA, Wunderink RG, Anzueto A, et al. Infectious Diseases Society of America/American Thoracic Society consensus guidelines on the management of community-acquired pneumonia in adults. Clin Infect Dis 2007;44(Suppl 2):S27-72. ↩︎
Li CF, Liu MF, Shi ZY, et al. Changing trends in antimicrobial susceptibility of Streptococcus pneumoniae isolates in Taiwan, 2006-2007. J Microbiol Immunol Infect 2012;45(4):305-10. ↩︎
Yzerman EP, Den Boer JW, Lettinga KD, et al. Sensitivity of three urinary antigen tests associated with clinical severity in a large outbreak of Legionnaires' disease in The Netherlands. J Clin Microbiol 2002;40(9):3232-6. ↩︎
Jensen JU, Hein L, Lundgren B, et al. Procalcitonin-guided interventions against infections to increase early appropriate antibiotics and improve survival in the intensive care unit: a randomized trial. Crit Care Med 2011;39(9):2048-58. ↩︎
Gibot S, Cravoisy A, Levy B, et al. Soluble triggering receptor expressed on myeloid cells and the diagnosis of pneumonia. N Engl J Med 2004;350(5):451-8. ↩︎
Oppert M, Reinicke A, Muller C, et al. Elevations in procalcitonin but not C-reactive protein are associated with pneumonia after cardiopulmonary resuscitation. Resuscitation 2002;53(2):167-70. ↩︎
Klein Klouwenberg PM, Van Mourik MS, Ong DS, et al. Electronic implementation of a novel surveillance paradigm for ventilator-associated events. Feasibility and validation. Am J Respir Crit Care Med 2014;189(8):947-55. ↩︎ ↩︎ ↩︎ ↩︎
Boyer AF, Schoenberg N, Babcock H, et al. A prospective evaluation of ventilator-associated conditions and infection-related ventilator-associated conditions. Chest 2015;147(1):68-81. ↩︎ ↩︎
Bouadma L, Sonneville R, Garrouste-Orgeas M, et al. Ventilator-Associated Events: Prevalence, Outcome, and Relationship With Ventilator-Associated Pneumonia. Crit Care Med 2015;43(9):1798-806. ↩︎ ↩︎ ↩︎ ↩︎ ↩︎ ↩︎
Fan Y, Gao F, Wu Y, et al. Does ventilator-associated event surveillance detect ventilator-associated pneumonia in intensive care units? A systematic review and meta-analysis. Crit Care 2016;20(1):338. ↩︎