第二章:社區型肺炎
2-5 治療評估及診斷流程
重點提要
社區型肺炎治療失敗包括治療後生命徵象不穩定或臨床惡化,早期(治療後 72 小時內)原因包括疾病的自然病程、藥物因素或診斷錯誤,晚期(治療後 72 小時以上)則包括疾病合併症、藥物因素或診斷錯誤。治療失敗時應再次評估診斷是否正確以及是否因為感染導致的併發症引起的治療失敗。反覆 的病史詢問、理學檢查,微生物檢驗(痰液革蘭氏染色及培養、抗原或抗體檢測)、影像學檢查、甚至侵入性檢查(如超音波導引肋膜液抽吸或肋膜切片、 氣管內視鏡檢)以獲得感染的致病原證據,為初始治療失敗之後續策略。
主編:詹明澄
副編:何茂旺
一、初始治療穩定(clinical stability)的診斷標準 [1]:
加入書籤
符合下列六項條件:體溫 < 37.8 °C,心跳 < 100/分鐘,呼吸速率 < 24/分鐘,收縮壓 > 90 mmHg,血氧飽和度 > 90%(FiO2:21%),能經口進食,意識正常 。
二、初始治療失敗定義 [2][3][4]:
加入書籤
(一)社區型肺炎:符合社區型肺炎定義之病人
具備下列任一臨床狀況即認定為治療失敗:
門診病患:已於門診接受抗生素治療,後因抗藥性或臨床療效不佳而需要調整抗生素或住院治療。
住院病患:
- 早期失敗:住院病人經抗生素治療,72 小時內出現臨床惡化(clinical deterioration),生命徵象不穩定,如持續性發燒、休克、呼吸情況惡化甚至衰竭或死亡。
- 晚期失敗:住院病人經抗生素治療,超過 72 小時後出現臨床惡化(clinical deterioration), 生命徵象不穩定,如持續性發燒、休克、呼吸情況惡化甚至衰竭或死亡。
三、處置建議
加入書籤
治療失敗時應再次評估診斷是否正確以及是否是因為感染導致的併發症引起的治療失敗。一般來說,感染症病人於初始治療須一段時間觀察反應。治療反應會因為疾病以及病人因素有所不同,目前文獻上 [1] 以三天作為分界線。
此外,肺炎為臨床診斷,其他疾病也可能有類似肺炎之表現。過去文獻指出,有約 12% 病患在治療過程中無法對抗生素有反應,後來證實為非感染之臨床 情況 [2][5]。另外心臟衰竭合併肺水腫甚至是非感染性的血管炎有時也會被誤認為肺炎而進行肺炎的治療,爾後會有治療反應不佳之情況發生。故治療失敗時應再次評估診斷是否正確以及是否是因為感染導致的併發症引起的治療失敗。表 2.5.1 為常見反應不佳之原因之整理。
表 2.5.1 社區型肺炎治療失敗的原因[1][6]
 註:BOOP,bronchiolitis obliterans organizing pneumonia 阻塞性細支氣管炎
註:BOOP,bronchiolitis obliterans organizing pneumonia 阻塞性細支氣管炎
(一)再次詳細詢問病史以及身體檢查評估(見圖 2.5.1 及圖 2.5.2)
如果發生治療反應不佳時,應再次詢問病史,包含 TOCC(travel 旅遊史、 occupation 職業史、contact 接觸史、cluster 群聚感染),並再一次進行身體檢查評估是否有新的病灶,例如:呼吸音變低沉暗示有肋膜積水需要做進一步化驗等 [4]。病史與相關病原如表 2.5.2:
表 2.5.2 病史與病原菌的相關性 [1]
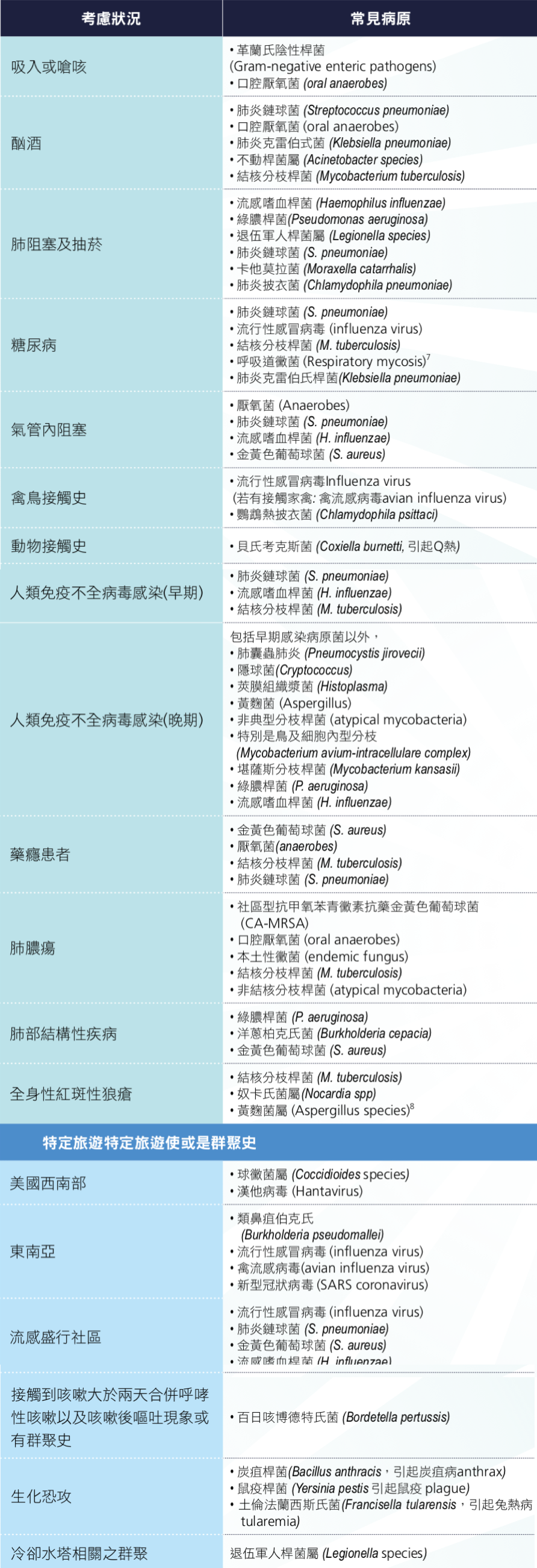
(二)宿主因素以及除細菌以外病原,包括病毒,黴菌及結核菌之可能性。
黴菌感染危險因子最重要為宿主因素,例如:血球低下,而非血球低下黴菌感染危險因子包括:長期大量使用類固醇,肺阻塞,肝硬化,住加護病房超過一星期,後天免疫缺乏症候群,肺移植等 [7][8][9][10][11] 。
其他宿主因素造成社區型肺炎疾病嚴重度增加或是治療失敗風險包括:年紀大,有喝酒或是抽菸 [3][12],一開始即為多葉性肺炎或有合併膿胸或是菌血症者,脾臟切除 [13],患有惡性腫瘤,患有神經學相關之疾病包含腦血管病變多發性硬化症,腦內腫瘤,退化性病變 [5][14]以及免疫抑制患者 [15]。
(三)實驗室檢驗
在治療失敗時,可考慮進行抽血檢驗 C-反應蛋白(C-reactive protein, CRP)或是前降鈣素(procalcitonin, PCT)搭配臨床作為臨床鑑別診斷之工具。不建議單獨只憑 CRP、PCT 來當作治療或是追蹤的單一考量。當治療失敗時,如果病患呈現低 CRP 或是低 PCT 時,則需要再考慮其他鑑別診斷 [16][17]。 且如果已經認為是感染相關治療失敗時不建議持續追蹤 CRP 跟 PCT 作為治療之成效評估。
必要時進行藥物濃度監測。治療失敗時應考慮藥物動力學之影響,有可能是藥物濃度不足造成治療失敗,尤其是使用胺基醣苷類(aminoglycosides)或萬古黴素(vancomycin)時需監測藥物濃度 [18]。
如果一開始沒有進行微生物抗原或是抗體測試時可考慮尿液抗原或血清學等臨床檢驗,包括:肺炎鏈球菌以及退伍軍人症尿液抗原檢驗(urinary antigen tests for Streptococcus pneumoniae and Legionella pneumophila),肺炎黴漿菌抗體檢驗(Mycoplasma pneumoniae antibody),和退伍軍人症血清抗體測定(Legionella antibody test)。
重新收集痰液作革蘭氏染色及病原菌培養(Good Practice)。
(四)影像學檢查
在治療失敗時可以考慮使用影像檢查,包括胸部 X 光,胸部超音波以及胸部電腦斷層 [4]。
(五)支氣管鏡檢查
在治療反應不佳患者,支氣管鏡可以搭配肺泡灌洗術及切片,提供更多的資訊,以協助鑑別診斷。(見 2.4. 診斷措施(二):呼吸道檢體)
圖 2.5.1 社區型肺炎診斷流程
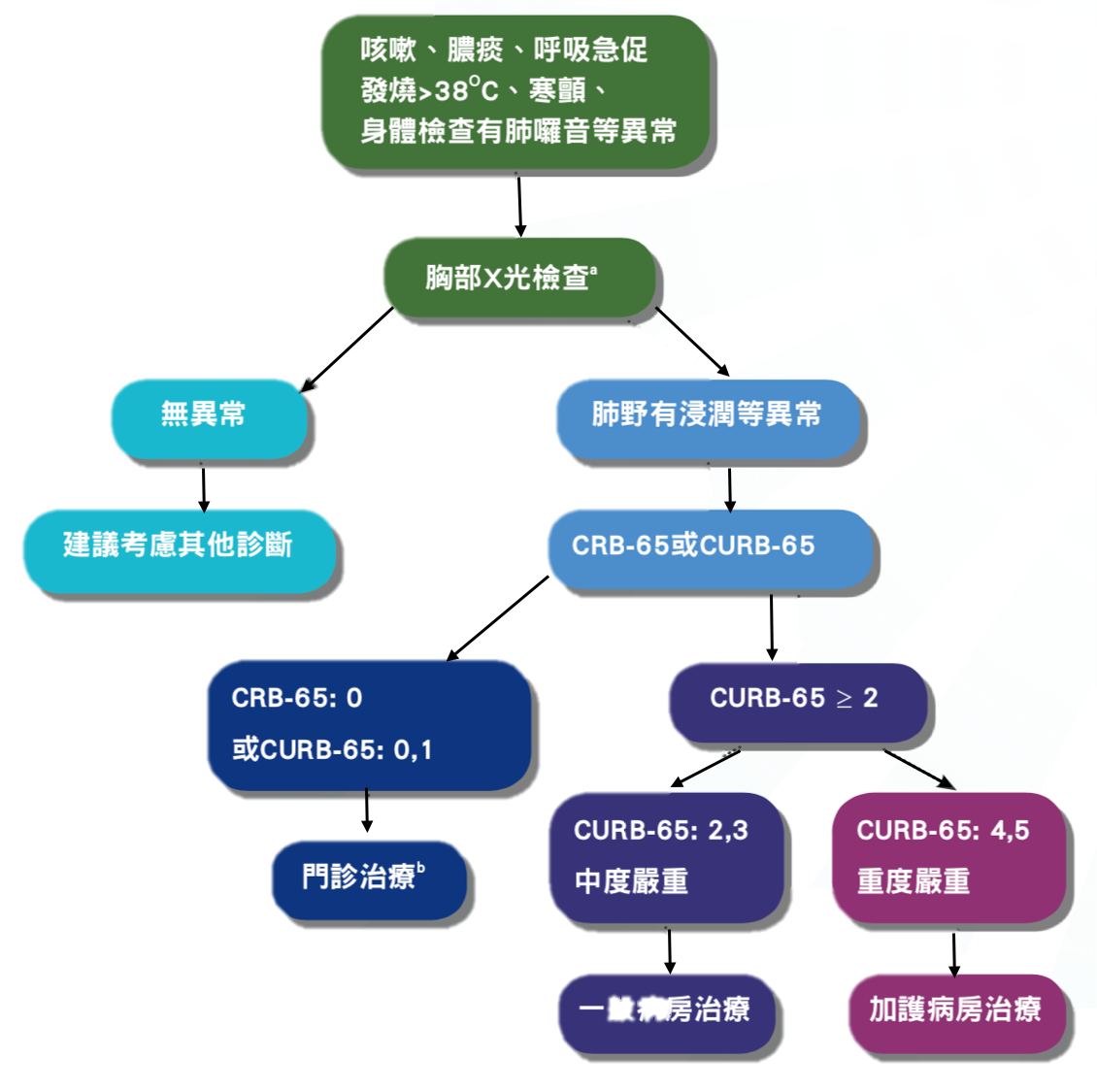 a 若無胸部X光片,可由臨床症狀判斷
b 若因共病,家庭照顧困難等因素,可考慮住院治療
a 若無胸部X光片,可由臨床症狀判斷
b 若因共病,家庭照顧困難等因素,可考慮住院治療
圖 2.5.2 社區型肺炎初始治療失敗診斷處置建議

四、參考文獻
加入書籤
Mandell LA, Wunderink RG, Anzueto A, et al. Infectious Diseases Society of America/American Thoracic Society consensus guidelines on the management of community-acquired pneumonia in adults. Clin Infect Dis 2007;44 Suppl 2:S27-72. ↩︎ ↩︎ ↩︎ ↩︎
Arancibia F, Ewig S, Martinez JA, et al. Antimicrobial treatment failures in patients with community-acquired pneumonia: causes and prognostic implications. Am J Respir Crit Care Med 2000;162(1):154-60. ↩︎ ↩︎
Menendez R, Torres A, Zalacain R, et al. Risk factors of treatment failure in community acquired pneumonia: implications for disease outcome. Thorax 2004;59(11):960-5. ↩︎ ↩︎
Martin-Loeches I Fau - Valles X, Valles X Fau - Menendez R, Menendez R Fau - Sibila O, et al. Predicting treatment failure in patients with community acquired pneumonia: a case-control study. Respir Res 2014(1465-993X (Electronic)). ↩︎ ↩︎ ↩︎
Genne D, Sommer R, Kaiser L, et al. Analysis of factors that contribute to treatment failure in patients with community-acquired pneumonia. Eur J Clin Microbiol Infect Dis 2006;25(3):159-66. ↩︎ ↩︎
Goncalves-Pereira J, Conceicao C, Povoa P. Community-acquired pneumonia: identification and evaluation of nonresponders. Ther Adv Infect Dis 2013;1(1):5-17. ↩︎
Meersseman W, Lagrou K, Maertens J, et al. Invasive aspergillosis in the intensive care unit. Clin Infect Dis 2007;45(2):205-16. ↩︎
De Pauw B, Walsh TJ, Donnelly JP, et al. Revised definitions of invasive fungal disease from the European Organization for Research and Treatment of Cancer/Invasive Fungal Infections Cooperative Group and the National Institute of Allergy and Infectious Diseases Mycoses Study Group (EORTC/MSG) Consensus Group. Clin Infect Dis 2008;46(12):1813-21. ↩︎
Jensen J, Guinea J, Torres-Narbona M, et al. Post-surgical invasive aspergillosis: an uncommon and under-appreciated entity. J Infect 2010;60(2):162-7. ↩︎
Munoz P, Ceron I, Valerio M, et al. Invasive aspergillosis among heart transplant recipients: a 24-year perspective. J Heart Lung Transplant 2014;33(3):278-88. ↩︎
Munoz P, Vena A, Ceron I, et al. Invasive pulmonary aspergillosis in heart transplant recipients: two radiologic patterns with a different prognosis. J Heart Lung Transplant 2014;33(10):1034-40. ↩︎
Roson B, Carratala J, Fernandez-Sabe N, et al. Causes and factors associated with early failure in hospitalized patients with community-acquired pneumonia. Arch Intern Med 2004;164(5):502-8. ↩︎
Tajiri T, Tate G, Enosawa T, et al. Clinicopathological findings in fulminant-type pneumococcal infection: report of three autopsy cases. Pathol Int 2007;57(9):606-12. ↩︎
Cilloniz C, Ewig S, Polverino E, et al. Community-acquired pneumonia in outpatients: aetiology and outcomes. Eur Respir J 2012;40(4):931-8. ↩︎
Pneumonia in immunocompromised patients. Respirology 2009;14 Suppl 2:S44-50. ↩︎
Balci C, Sungurtekin H, Gurses E, et al. Usefulness of procalcitonin for diagnosis of sepsis in the intensive care unit. Crit Care 2003;7(1):85-90. ↩︎
Povoa P, Coelho L, Almeida E, et al. C-reactive protein as a marker of infection in critically ill patients. Clin Microbiol Infect 2005;11(2):101-8. ↩︎
Rhodes A, Evans LE, Alhazzani W, et al. Surviving Sepsis Campaign: International Guidelines for Management of Sepsis and Septic Shock: 2016. Intensive Care Med 2017;43(3):304-77. ↩︎