第二章:社區型肺炎
2-2 特殊病原菌之診斷時機
重點提要
社區型肺炎需要考量到的特殊病原菌的時機,除在細菌性抗生素治療失敗時,還包括當病人為免疫不全宿主,特別是近年來使用腫瘤壞死因子阻斷劑類藥品必須特別考慮肺結核復發,另外吸入型類固醇也有實證會增加肺炎風險。還有在不同流行季節或地域需考慮到新興傳染病及疫情,如季節性和新興流行性感冒、如台灣南部地區雨季或水災後易有類鼻疽肺炎等。近年來流感重症後肺炎有發生侵襲性麴菌肺炎。診斷方法沒有太多更新,主要是在快速診斷和分子診斷方面的發展。
主編:李欣蓉
副編:許超群
一、特殊病原菌簡介
加入書籤
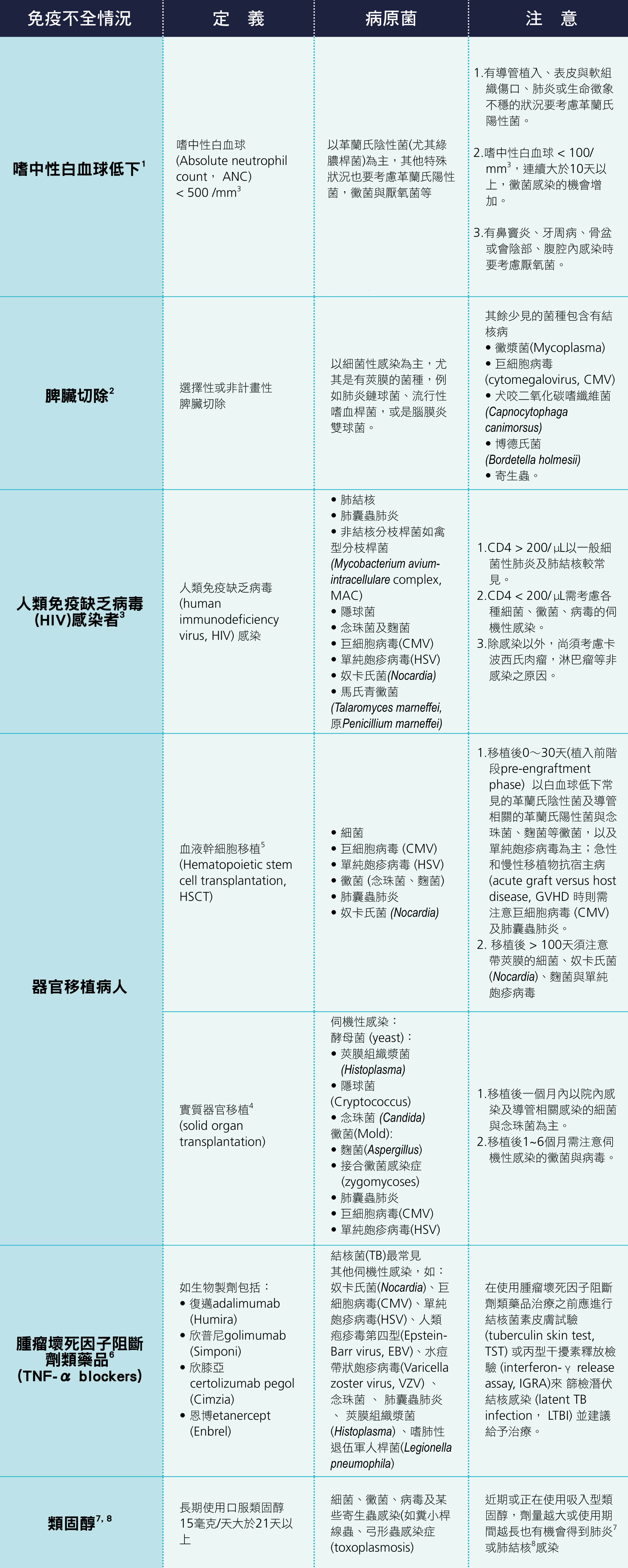
社區型肺炎需要考量到特殊病原菌的時機包括當病人為免疫不全宿主,如嗜中性白血球低下 [1]、脾臟切除 [2]、人類免疫缺乏病毒(human immunodeficiency virus, HIV)感染者 [3]、及使用免疫製劑如器官移植患者 [4][5]、使用腫瘤壞死因子阻斷劑類藥品(tumor necrosis factor-alpha(TNF-α)blockers)[6]或全身性或吸入性類固醇 [7][8]等(見表 2.2.1)。其他特殊病原菌包括病毒性肺炎如流行性感冒病毒、冠狀病毒引起之嚴重急性呼吸道症侯群(severe acute respiratory syndrome, SARS)和中東呼吸症候群(Middle East respiratory syndrome, MERS),黴菌性肺炎如隱球菌及麯菌肺炎,肺囊蟲肺炎,類鼻疽肺炎,肺結核及非結核分枝桿菌肺炎。
表 2.2.1 免疫不全之宿主易感染之特殊病原菌
二、病毒性肺炎
加入書籤
下呼吸道病毒感染可引發哮吼、細支氣管炎、氣管支氣管炎、氣喘或慢性阻塞性肺病之急性發作、肺炎等臨床病癥。病毒性肺炎即是指病毒引發肺部實質的發炎,通常會在影像檢查呈現異狀,並伴隨肺泡氣體交換功能異常,隨著病毒特 性、宿主的年齡與免疫力等因素,會有差異很大的臨床表現。在平時健康的成年人,大多僅有流行性感冒肺炎以純粹的病毒性肺炎表現;年長者病毒性肺炎的發生率與一般成年人差不多,但常有較多下呼吸道症狀,甚至在平時健康的成年人只引發上呼吸道感染的病毒也可能在年長者引發肺炎。
(一)病毒性肺炎診斷時機
在免疫力正常成年人病毒性肺炎常見的病原包括:流行性感冒病毒、呼吸道融合病毒、副流行性感冒病毒、腺病毒、麻疹病毒、水痘帶狀皰疹病毒等;在免疫功能不全病人,有較多種類的病毒(包括:人類巨細胞病毒、單純皰疹病毒、水痘帶狀皰疹病毒、腺病毒、呼吸道融合病毒、副流行性感冒病毒、流行性感冒病毒、鼻病毒等)均可引發病毒性肺炎,發病率與死亡率也較高。心肺疾病(特別是瓣膜性心臟病、慢性阻塞性肺病等)是病毒性肺炎的危險因子,孕婦(特別是在第二、三孕程)也常會因流行性感冒肺炎引發心肺併發症而住院 [9]。
成人的病毒性肺炎常以發燒及乾咳表現,有時會伴隨結膜炎、鼻炎等症狀,某些嚴重的病毒性肺炎會有粉紅色泡沫痰,甚至會伴隨低血氧、發紺等現象。身體檢查常無特異性發現,通常病人呈現急性病態、呼吸急促,胸部聽診常可聽到瀰漫性鑼音或喘鳴音。在胸部 X 光上常以雙側瀰漫性間質性肺浸潤為主,但也可能以大葉性浸潤的表現,因此往往無法輕易與細菌性肺炎區分。痰液少,抹片通常僅可見少量多核球與極少量的細菌 [9]。成人病毒性肺炎常同時伴隨細菌性肺炎,若在典型病毒感染症狀改善的 2~14 天內重新產生發燒、咳嗽或呼吸困難等症狀,須考慮到繼發性細菌感染,發生率約 26~77%。流行性感冒後常見引起繼發性感染的細菌主要為肺炎鏈球菌(Streptococcus pneumoniae), 而 S. aureus 與流感嗜血桿菌(Haemophilus influenzae)亦頗常見 [9]。
(二)病毒性肺炎診斷方法
由於不易取得適當檢體來做培養或病毒分離,常無法藉此確認確切病因或病毒種類,尤其是一些病毒(如疱疹病毒、腺病毒等)在全身散布時常無症狀,更難掌握適當採檢時機。血清學檢查可以協助了解時序性,但無法確認病毒與症狀 的因果關係,在高盛行時期更是容易誤導判斷。總歸而言,病毒性肺炎的表現除了病毒本身之外,宿主的年齡與免疫力狀態是主要決定因素 [9]。
一般門診的感冒症狀不需作病毒檢測,但在流感流行期間住院的重度肺炎、符合防疫單位採檢規定(如「H5N1 病毒採檢定義」)或有群聚現象等情況,為了防止病原散播並早期投予抗病毒藥物治療,應做流行性感冒病毒檢測。病毒檢 測可取鼻咽拭子(nasopharyngeal swab)、喉拭子(throat swab)、鼻抽取液(nasal aspirate)或支氣管抽取液(bronchial aspirate)作病毒培養(viral culture)、快速抗原檢測(rapid antigen test)、直接螢光抗體(direct fluorescent antibody, DFA)或酵素免疫分析(enzyme immunoassay, EIA)、或即時聚合酶鏈鎖反應(RT-PCR),或血清抗體分析。其中以抗原檢測最為快速,可在 30 分鐘內得到結果(DFA 與 EIA 要 2~4 小時;RT-PCR 要 1~2 天;病毒培養要 3~10 天;血清抗體要兩週以上)。若以人類流感病毒培養結果作為參考基準,快速檢驗的敏感度約為 70%,專一性約為 90%。如果在流感流行期間對於具有典型症狀與明顯接觸史的病人進行檢測,可大大增加其診斷的敏感度。快速抗原檢驗對 H5N1 病毒的敏感度偏低 [9][10]。
三、真菌肺炎
加入書籤
(一)隱球菌肺炎
隱球菌為一帶有莢膜之真菌,在免疫不全或免疫正常的人身上都可能造成隱球菌感染(cryptococcosis)。隱球菌感染為目前死亡率最高的一種侵襲性黴菌感染,在全世界每年超過一百萬的感染病人當中,約造成 65 萬人死亡 [11][12]。在 70 種(species)隱球菌中,主要造成人類感染的菌種為新型隱球菌(Cryptococcus neoformans )及格特隱球菌(Cryptococcus gattii),其中新型隱球菌分佈全球,多存在於土壤中且會經由鳥類,如鴿子及雞傳播而散佈,而格特隱球菌原本被認為大多存在於熱帶及亞熱帶區域,但近年來在北美太平洋沿岸北部地區亦發現增多案例 [13][14]。在台灣,經統計在 1997 年至 2010 年間,超過 95% 的隱球菌感染之病原菌為新型隱球菌,而其餘感染皆由格特隱球菌所造成 [15]。
隱球菌肺炎診斷時機
隱球菌肺炎的臨床表現變化多端,可以是無症狀的感染也可能以嚴重肺炎併呼吸衰竭表現。在無免疫低下狀況的病人中,隱球菌肺炎多侷限在肺部感染,大部分沒有症狀,或以非特異性症狀如發燒、全身倦怠、咳嗽帶痰及喘來表現 [11][14]。如為人類免疫不全病毒(Human Immunodeficiency Virus, HIV)感染病人,隱球菌肺炎較好發在 CD4 T 淋巴球小於 100 cells/mL 的病人 [3]。如為單純隱球菌肺炎,臨床上則大多以非特異性症狀為主,但在此群病人身上通常合併有其他全身性隱球菌感染,特別是隱球菌腦膜炎,因此多合併其他系統性症狀如頭痛等,亦可能因嚴重感染呈現呼吸衰竭的情形 [13][16]。隱球菌肺炎在肺部影像上的表現和宿主的免疫程度相關。在無免疫低下狀況的病人,電腦斷層上的異常多以肺部團塊(solitary mass)或多發性肺部小結節(nodules)來表現,亦常見肺部實質化(consolidation),其他如肋膜積水、空洞化、或間質性病變偶爾亦可見。而在免疫不全的病人上較少見侷限性的結節,多以彌漫性病變、肋膜積水、空洞化病灶或肺部實質化為主 [13]。
由於隱球菌感染與宿主免疫情況高度相關,如肺炎病人有以下危險因子時,應考慮是否有隱球菌肺炎之可能:愛滋病(特別在 CD4 T 淋巴球 < 100 cells/μL 時)、自體免疫疾病、使用免疫抑制劑、曾經使用類固醇、血液腫瘤疾病、癌症、肝硬化、肺部疾病、糖尿病等 [15][17]。
隱球菌肺炎診斷方法
隱球菌肺炎的診斷須具備三個條件:疑似臨床症狀、影像學表現,及在痰液 中染色或培養出隱球菌。痰液細胞學染色檢查及病理檢驗亦可輔助診斷。隱球菌抗原檢驗(cryptococcus antigen),在全身性隱球菌感染及隱球菌腦膜炎為一敏感且具特異性之檢查工具,但如為單純隱球菌肺部感染,檢驗結果通常為陰性,無法使用來作為隱球菌肺炎之診斷工具。如在隱球菌肺炎病人得到隱球菌抗原陽性結果,須考慮是否有全身性隱球菌感染的可能性。此外,在免疫不全病人中,如有診斷為隱球菌肺炎,須同時進行全身性隱球菌感染的檢查,包括腦脊髓液及血液的隱球菌培養和隱球菌抗原檢驗 [11][13][14]。
(二)侵襲性麴菌肺炎
侵襲性麴菌感染為目前造成伺機性肺炎最常見的黴菌(mold)。在超過 900 種(species)的麴菌中,對人類有致病力者最常見的兩種為薰煙麴菌(Aspergillus fumigatus)及黃麴菌(Aspergillus flavus),其餘則有黑麴菌(Aspergillus niger)、小巢狀麴菌(Aspergillus nidulans)、土麴菌(Aspergillus terreus)及曲麴菌(Aspergillus ustus)等。麴菌遍佈世界各地,存在於土壤、水、空氣及腐生植物中,可於免疫不全或肺部構造病變的病人造成侵襲性肺部感染 [14]。在台灣,侵襲性麴菌感染為侵襲性真菌感染中的最大宗 [12]。於文獻中統計,台灣 2000 年到 2009 年造成侵襲性麴菌感染最多的病原菌為薰煙麴菌(A. fumigatus)及 黃麴菌(A. flavus),總共佔了所有感染中的八成 [18]。
侵襲性麴菌肺炎診斷時機
要診斷侵襲性麴菌肺炎相當困難,在感染早期往往沒有明顯症狀,主要為發燒、咳嗽、咳血及胸痛等非特異性表現。若合併有其他部位的感染,則可能會有中樞神經,皮膚等臨床病灶。感染部位與宿主本身疾病及免疫狀況有很大關係,如為血液惡性疾病病人,侵襲性麴菌感染多為全身性感染 [14]。影像學上,侵襲性麴菌肺炎在肺部電腦斷層上的典型病灶為肺部結節及實質化病變(consolidation)。在嗜中性球低下病人中,如在電腦斷層上見到肺部結節併周圍毛玻璃狀病灶(halo sign),或見肺部結節併開洞病灶(air crescent sign)皆須考慮有肺部麴菌感染之可能性。
侵襲性麴菌肺炎好發於免疫不全及有慢性疾病或重症之病人。如肺炎病人有以下危險因子,需考慮是否有侵襲性麴菌肺炎之可能 [12][14][19]:(i)免疫不全:血液惡性疾病、嗜中性球低下時間過久、長期類固醇使用、骨髓移植、器官移植、巨細胞病毒感染等。(ii)其他:加護病房病人、慢性肺病、肝硬化、洗腎。
侵襲性麴菌肺炎診斷方法
侵襲性麴菌肺炎的診斷以培養結果及病理檢驗為確診依據。在特定族群,如血液惡性疾病及骨髓移植病人,亦可進行血清及支氣管沖洗液的半乳甘露聚糖檢驗(galactomannan test)確認診斷。另外在歐美國家亦會採行血清檢驗(1 → 3)-β-D-glucan 於特定族群病人診斷侵襲性麴菌肺炎,但於台灣臨床醫療常規中無此檢驗項目,且此法檢驗特異性較低 [19]。臨床問題:在臨床上懷疑有侵襲性麴菌肺炎的病人,是否應進行支氣管鏡檢查以輔助診斷?如病人在臨床上懷疑有侵襲性麴菌肺炎,則應審慎評估病人之臨床狀況,考慮行支氣管鏡檢查併支氣管肺泡灌洗,並進行灌洗液之培養以增加麴 菌感染的診斷率 [19]。
(三)肺囊蟲肺炎
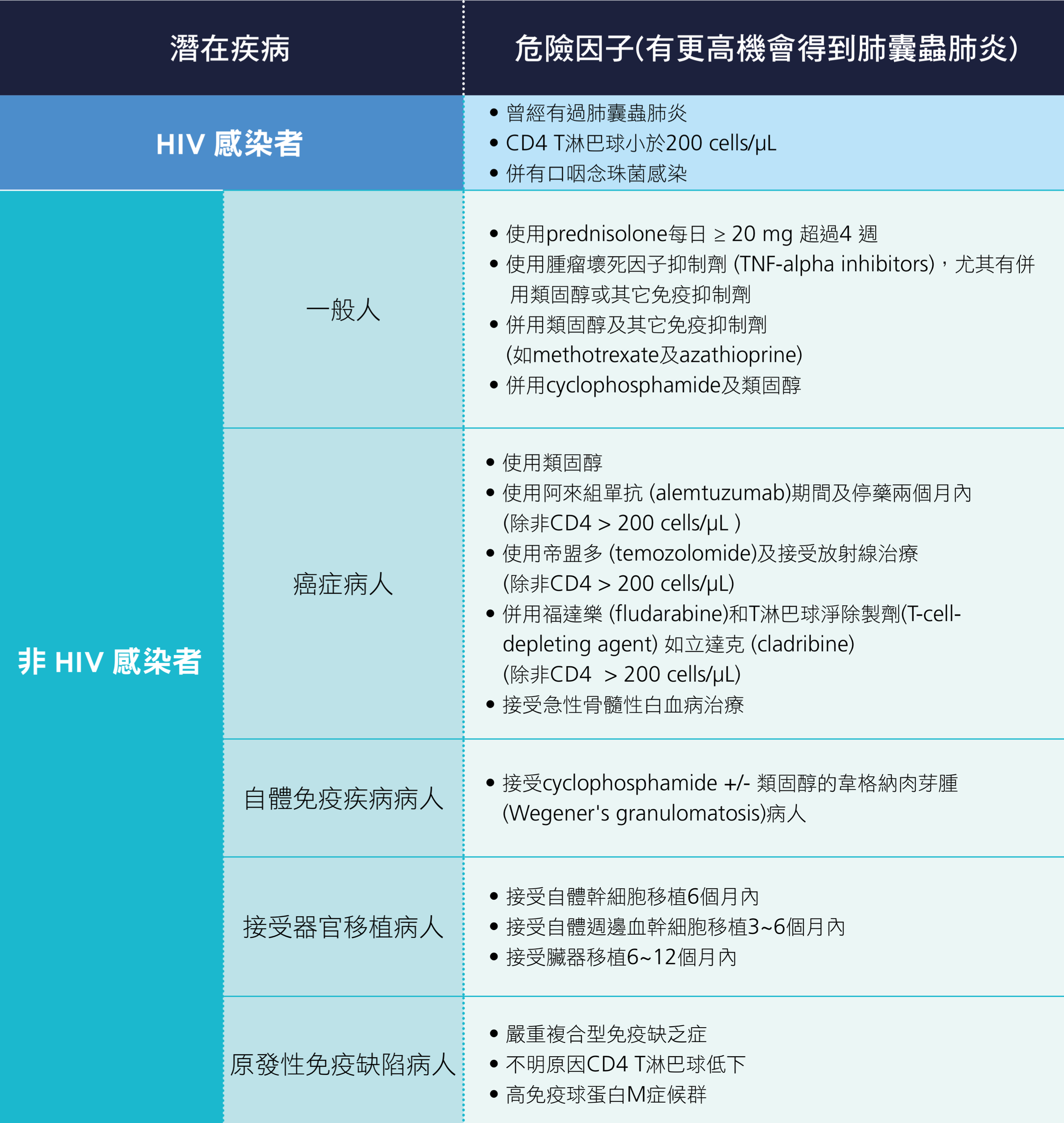
肺囊蟲肺炎(Pneumocystis pneumonia, PCP)是由名為卡式肺囊蟲(Pneumocystis jirovecii )的真菌所致,主要發生在免疫力低下的宿主(見表 2.2.2)。大部分個案發生在 HIV 感染者 [5]。在沒有抗反轉錄病毒藥物治療(antiretroviral therapy, ART)治療時代,PCP 的發生率約 70~80%,死亡率約 20~40%。但在有 ART 以及 PCP 預防用藥後,發生率大幅下降,死亡率也下降至 10~12%。在非 HIV 感染者如惡性腫瘤、接受器官移植病人、自體免疫疾病病人、發炎性腸道疾病(Inflammatory bowel disease, IBD)病人等,因為化學治療或免疫抑制劑使用,發生率漸增,死亡率約 30~50%。
表 2.2.2 肺囊蟲肺炎感染之危險因子
肺囊蟲肺炎診斷時機
在所有免疫低下病人的肺炎,都應該要考慮肺囊蟲肺炎的可能性。以下將免疫低下的病人分為 HIV 感染者及非 HIV 感染者 [20][21]:(i)HIV 感染者:病程較亞急性或慢性,症狀常為漸進的喘、乾咳、低燒及倦怠。可能侵犯肺部以外,包括眼睛、淋巴結、骨髓、甲狀腺、肝、脾、腎等器官。(ii)非 HIV 感染者:病程較急性( 平均 7 天 ),症狀除乾咳及喘,更常快速進展到呼吸衰竭,高燒,較少有肺外症狀。肺囊蟲肺炎診斷方式
影像學上,典型胸部 X 光表現為雙側間質性浸潤,但在疾病早期也可以是正常的。胸部電腦斷層可見以狀塊分佈的瀰漫性毛玻璃陰影(ground-glass opacity, GGO),也可能出現囊性病變。一般實驗室檢查較常見或稍具特異性的表現有動脈血氧氧合不足、血液中乳酸脫氫酶(lactate dehydrogenase, LDH)升高。
表 2.2.3 肺囊蟲肺炎診斷方式
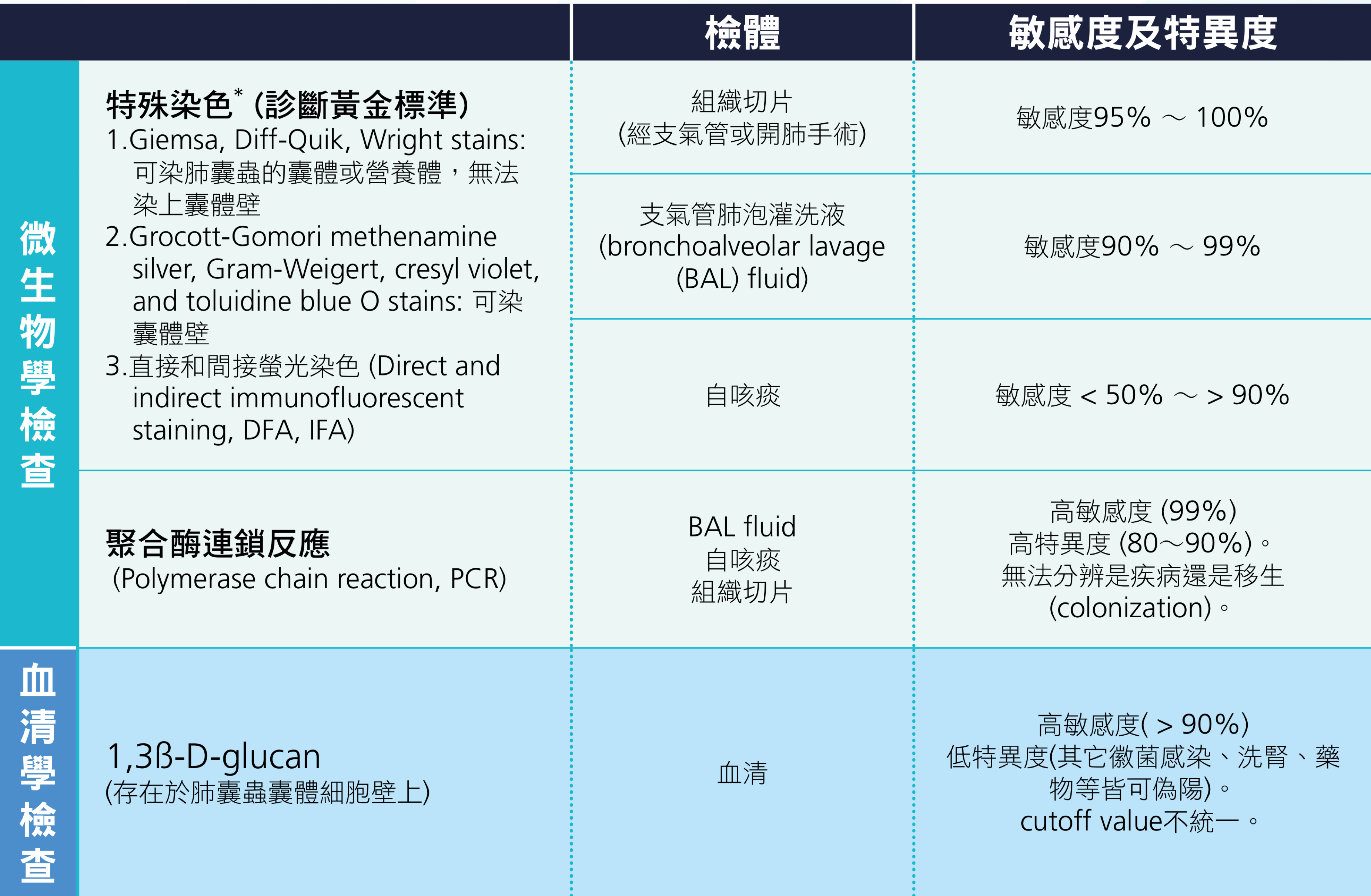 * 在非 HIV 感染者的肺囊蟲肺炎,通常病原體數量較少,因此偽陰性機會較高。
* 在非 HIV 感染者的肺囊蟲肺炎,通常病原體數量較少,因此偽陰性機會較高。
四、類鼻疽肺炎
加入書籤
類鼻疽是感染類鼻疽柏克氏菌(Burkholderia pseudomallei)所致,此菌存在於土壤和積水環境,而疾病的發生常和降雨氣候相關,例如颱風時節。好發在全球熱帶及亞熱帶地區,包括新加坡、馬來西亞、泰國、澳洲等,其中台灣也屬好發地區。其病程可以急性到慢性,少部分可以潛伏人體多時再發病。急性疾病常見的形式即為肺炎及菌血症,死亡率高。
(一)類鼻疽肺炎診斷時機
急性類鼻疽肺炎平均潛伏期為 9 天,且常合併有菌血症(40 ∼ 60%) 和敗血性休克(20%),甚至快速進展成呼吸衰竭。多發生在雨季、颱風季節,病人平均年紀在 44 歲。八成的病人有一種以上的慢性疾病或危險因子 [22]:糖尿病(23% ~ 60%)、酗酒(12% ∼ 39%)、慢性腎臟病(10% ∼ 27%)、慢性肺部疾病(12% ∼ 27%)、地中海貧血(7%)、非典型的分枝桿菌疾病、類固醇或其它免疫抑制劑(<5%)、癌症(< 5%)。也需注意有機會接觸泥土及水的職業史或暴露史。
(二)類鼻疽肺炎診斷方法
胸部影像學上變化萬千如偉大的模仿者。急性類鼻疽肺炎最常見實質化或多發結節併肺泡浸潤,多見於上肺野,可以合併開洞或膿胸 [23]。除胸部外,類鼻疽可以經血行到肺外產生膿瘍,常見有脾、肝、腦等。
表 2.2.4 類鼻疽肺炎診斷方法
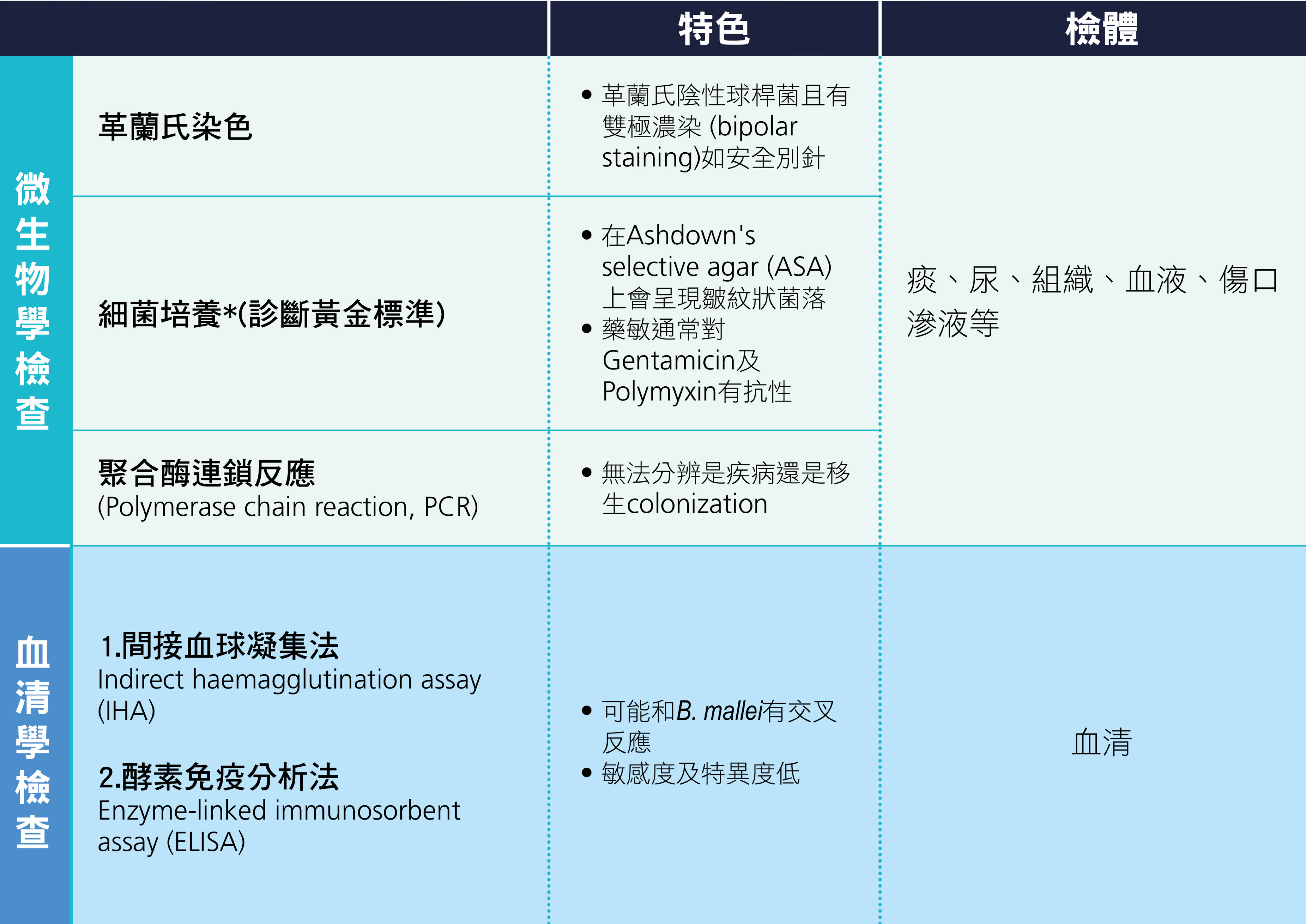
五、肺結核
加入書籤
人類的結核病多由結核分枝桿菌(Mycobacterium tuberculosis)所引起。結核分枝桿菌生長緩慢,約 20 小時分裂一次,需要數週的時間培養,其細胞壁富含脂質,不容易被染色,但一旦染上色就不易被強酸脫色,為耐酸性桿菌。我國結核病的發生率於 2015 年為每十萬人口 46 人。關於結核病詳細的診斷治療介紹,請參考由衛生福利部台灣疾病管制署出版之結核病診治指引 [24]。
(一)肺結核的診斷時機
在以下幾種情形,須懷疑病人有肺結核、或具有較高肺結核的可能性:
- 具有肺結核的臨床症狀:肺結核最主要的症狀為咳嗽,尤其是帶有黏液痰、大於 2 週以上的持續性咳嗽,其他症狀還有發燒、盜汗、體重減輕、食慾不振、咳血等。病人具備越多項以上症狀,肺結核的機率就越高。
- 初始診斷為肺炎,但經過適當抗生素治療後,症狀或肺部影像卻沒有完全緩解。
- 肺部影像有疑似活動性肺結核病灶:如空洞性病灶、單側或雙側的上肺野浸潤、肺炎病灶發生於上肺葉的頂段及後段,或下肺葉的上段時。
- 以下族群之結核病發生率較大眾為高:HIV 感染者、接受器官移植者、服用抗腫瘤壞死因子阻斷劑(Anti-TNFα)者、慢性腎病變及洗腎病人、體重過輕者( 體重指數 body mass index, BMI < 18.5)、接受過胃切除或小腸繞道手術者、長期使用類固醇者、糖尿病病人、酒癮病人、長期抽菸者 [24][25]。
- 具有特定環境或職業暴露史者:如活動性肺結核病人之居家或密切接觸者、曾暴露於矽土(silica)者、醫療工作者 [25]。
(二)肺結核的診斷方式
肺結核的診斷需要綜合病人的病史與症狀、肺部影像學檢查、以及微生物學檢驗三者,加以判定診斷:
- 病史詢問:詢問病人的臨床症狀、職業史、暴露史等。
- 胸部影像學檢查:懷疑有肺結核的病人,建議皆需進行胸部 X 光檢查。當胸部 X 光有異常時,最好能跟過去的 X 光進行比較,若有需要,胸部電腦斷層可提供比胸部 X 光更精確的影像與豐富的資訊。
- 痰液耐酸性染色鏡檢(簡稱痰液塗片):懷疑有肺結核時建議進行至少 2 套、 最好 3 套的痰液塗片檢查,且至少有 1 套為清晨之痰液 [24][26]。
- 痰液培養:由痰液培養出結核分枝桿菌,是 100% 確診肺結核的方式,但此方法最大的限制在於其時效性。一般需至少 1 週,多則 8 週的時間方能獲得報告。
- 核酸增幅檢驗(nucleic acid amplification test, NAAT):此技術可大幅降低偵測結核菌之門檻,並在數小時內完成檢驗。NAAT 在痰液塗片陽性時,敏感度高達 90% 以上,特異度 95% 以上;痰液塗片陰性時,敏感度降低至 40~93%,特異度維持在 95% 以上 [24]。世界衛生組織,以及我國結核病診治指引,皆建議針對所有懷疑肺結核的病人,常規進行 NAAT [24][25]。以下簡述 NAAT 分別在痰液塗片陽性及陰性時,展現出的診斷價值:
- 當痰液塗片陽性時,NAAT 可迅速分辨結核分枝桿菌或非結核分枝桿菌。若痰液塗片陽性,NAAT 也陽性,可直接診斷肺結核,立刻予以治療;若痰液塗片陽性,NAAT 陰性,則很可能是非結核分枝桿菌,可避免病人接受不必要的抗結核藥物治療。
- 當痰液塗片呈陰性時,NAAT 因為可偵測到數量更少的結核菌,可做為提高診斷率的工具。也就是當痰液塗片陰性,NAAT 陽性時,要仔細考慮病人很可能仍有肺結核。
- GeneXpert MTB/RIF:在各種不同的 NAAT 方式中,GeneXpert MTB/RIF 是 WHO 目前唯一建議的即時 NAAT 套組,可在一般實驗室的環境下、2 小時內獲得檢驗結果,對於痰液塗片陽性的檢體,敏感度為 98%、特異度 99%,對於痰液塗片陰性的檢體,敏感度降低為 68%,特異度仍高達 99%,並能同時偵測 rifampin 的抗藥性基因 [24]。
六、非結核分枝桿菌肺炎
加入書籤
Nontuberculous mycobacteria(NTM)是一群嗜氧、非移動性的微生物,廣泛地存在於周遭環境,尤其是土壤及水環境,NTM 一般來說致病性不高,即使日常生活中偶爾接觸到,也不易遭受感染。但當宿主的身體構造出現異常、或免疫力出現缺陷時,NTM 感染的機會就會增加。近年來,我國 NTM 在肺部移生及造成肺部疾病的發生率有上升趨勢。
(一)肺部 NTM 疾病(pulmonary NTM disease)的診斷時機
以下情形要懷疑病人有肺部 NTM 疾病:
- 具有肺部 NTM 疾病的症狀:雖然肺部 NTM 疾病臨床表徵多變,亦常不具特異性,但幾乎所有的病人都會有慢性咳嗽,其他症狀還有疲勞、發燒、有痰、氣促、咳血、胸痛、體重減輕等。
- 具有肺部構造異常的病人:例如陳舊性肺結核、慢性阻塞性肺病(chronic obstructive pulmonary disease, COPD)、支氣管擴張症(bronchiectasis)、囊性纖維化(cystic fibrosis),塵肺症(pneumoconiosis)等 [27][28]。
- 免疫功能出現缺陷者:例如接受器官移植病人、長期服用免疫抑制劑者、服用腫瘤壞死因子阻斷劑類藥品(TNF-α blockers)者、HIV 感染者、具白血球介素 12(interleukin-12)、丙型干擾素 interferon-γ(IFN-γ)、或 TNF-α 相關細胞激素傳導途徑缺陷者、體內有抗丙型干擾素自身抗體(anti-IFNγ autoantibody)者等 [29]。
- 具有相符合的肺部影像學病人:肺部 NTM 疾病肺部影像大致可分成兩大類,其一是以纖維化 / 開洞(fibrocavitary)來表現,另一類是以小結節 / 支氣管擴張(nodular/bronchiectatic)來表現。前者比較容易經由胸部 X 光發現病灶,後者有時單靠胸部 X 光仍不易發現,需要胸部電腦斷層方能看清楚病灶。
- 初始診斷為肺炎,但經適當抗生素治療後,症狀或肺部影像卻沒有完全緩解者。
(二)肺部 NTM 疾病(pulmonary NTM disease)的診斷方式
要診斷肺部 NTM 疾病需同時符合以下三個面向 [28][30]:
- 臨床症狀:符合的肺部症狀,且排除可能造成這些症狀的其他病因。
- 微生物學證據:至少兩套痰液培養、或是一套經由支氣管鏡沖洗取得的呼吸道檢體,長出 NTM;或是肺部病理切片符合分枝桿菌感染的變化,且其切片檢體培養出 NTM。
- 影像學:胸部 X 光、或胸部電腦斷層有符合 NTM 疾病之影像變化。
七、參考文獻
加入書籤
Freifeld AG, Bow EJ, Sepkowitz KA, et al. Clinical practice guideline for the use of antimicrobial agents in neutropenic patients with cancer: 2010 Update by the Infectious Diseases Society of America. Clin Infect Dis 2011;52(4):427-31. ↩︎
Davies JM, Lewis MP, Wimperis J, et al. Review of guidelines for the prevention and treatment of infection in patients with an absent or dysfunctional spleen: prepared on behalf of the British Committee for Standards in Haematology by a working party of the Haemato-Oncology task force. Br J Haematol 2011;155(3):308-17. ↩︎
Panel on Opportunistic Infections in Hiv-Infected Adults and Adolescents. Guidelines for the prevention and treatment of opportunistic infections in HIV-infected adults and adolescents: recommendations from the Centers for Disease Control and Prevention, the National Institutes of Health, and the HIV Medicine Association of the Infectious Diseases Society of America. Accessed Mar 7, 2018. ↩︎ ↩︎
Chakinala MM, Trulock EP. Pneumonia in the solid organ transplant patient. Clin Chest Med 2005;26(1):113-21. ↩︎
Soubani AO, Miller KB, Hassoun PM. Pulmonary complications of bone marrow transplantation. Chest 1996;109(4):1066-77. ↩︎ ↩︎
Baddley JW, Cantini F, Goletti D, et al. ESCMID Study Group for Infections in Compromised Hosts (ESGICH) Consensus Document on the safety of targeted and biological therapies: an infectious diseases perspective (Soluble immune effector molecules [I]: anti-tumour necrosis factor-alpha agents). Clin Microbiol Infect 2018;24(Suppl 2):S10-S20. ↩︎
Brassard P, Suissa S, Kezouh A, et al. Inhaled corticosteroids and risk of tuberculosis in patients with respiratory diseases. Am J Respir Crit Care Med 2011;183(5):675-8. ↩︎
Wang CY, Lai CC, Yang WC, et al. The association between inhaled corticosteroid and pneumonia in COPD patients: the improvement of patients' life quality with COPD in Taiwan (IMPACT) study. Int J Chron Obstruct Pulmon Dis 2016;11:2775-83. ↩︎
2015. Fishman's Pulmonary Diseases and Disorders. In Fishman's Pulmonary Diseases and Disorders, eds. MA Grippi, JA Elias, JA Fishman, RM Kotloff, AI Pack, RM Senior & MD Siegel. United States of America: McGraw-Hill Education. ↩︎ ↩︎ ↩︎ ↩︎ ↩︎
台灣衛生福利部疾病管制署網站資料. Accessed Jan 29. ↩︎
Schmiedel Y, Zimmerli S. Common invasive fungal diseases: an overview of invasive candidiasis, aspergillosis, cryptococcosis, and Pneumocystis pneumonia. Swiss Med Wkly 2016;146:w14281. ↩︎ ↩︎ ↩︎
Kung HC, Huang PY, Chen WT, et al. 2016 guidelines for the use of antifungal agents in patients with invasive fungal diseases in Taiwan. J Microbiol Immunol Infect 2018;51(1):1-17. ↩︎ ↩︎ ↩︎
Brizendine KD, Baddley JW, Pappas PG. Pulmonary cryptococcosis. Semin Respir Crit Care Med 2011;32(6):727-34. ↩︎ ↩︎ ↩︎ ↩︎
Smith JA, Kauffman CA. Pulmonary fungal infections. Respirology 2012;17(6):913-26. ↩︎ ↩︎ ↩︎ ↩︎ ↩︎ ↩︎
Tseng HK, Liu CP, Ho MW, et al. Microbiological, epidemiological, and clinical characteristics and outcomes of patients with cryptococcosis in Taiwan, 1997-2010. PLoS One 2013;8(4):e61921. ↩︎ ↩︎
Huang L, Crothers K. HIV-associated opportunistic pneumonias. Respirology 2009;14(4):474-85. ↩︎
Mirza SA, Phelan M, Rimland D, et al. The changing epidemiology of cryptococcosis: an update from population-based active surveillance in 2 large metropolitan areas, 1992-2000. Clin Infect Dis 2003;36(6):789-94. ↩︎
Hsiue HC, Wu TH, Chang TC, et al. Culture-positive invasive aspergillosis in a medical center in Taiwan, 2000-2009. Eur J Clin Microbiol Infect Dis 2012;31(7):1319-26. ↩︎
Patterson TF, Thompson GR, 3rd, Denning DW, et al. Practice Guidelines for the Diagnosis and Management of Aspergillosis: 2016 Update by the Infectious Diseases Society of America. Clin Infect Dis 2016;63(4):e1-e60. ↩︎ ↩︎ ↩︎
Tasaka S, Tokuda H. Pneumocystis jirovecii pneumonia in non-HIV-infected patients in the era of novel immunosuppressive therapies. J Infect Chemother 2012;18(6):793-806. ↩︎
Carmona EM, Limper AH. Update on the diagnosis and treatment of Pneumocystis pneumonia. Ther Adv Respir Dis 2011;5(1):41-59. ↩︎
Kingsley PV, Arunkumar G, Tipre M, et al. Pitfalls and optimal approaches to diagnose melioidosis. Asian Pac J Trop Med 2016;9(6):515-24. ↩︎
Burivong W, Wu X, Saenkote W, et al. Thoracic radiologic manifestations of melioidosis. Curr Probl Diagn Radiol 2012;41(6):199-209. ↩︎
衛生福利部台灣疾病管制署. 結核病診治指引第六版. 2017. last accessed Mar 7, 2018. ↩︎ ↩︎ ↩︎ ↩︎ ↩︎ ↩︎
W.H.O. Systematic screening for active tuberculosis: principles and recommendations. Placed Published: Geneva, Switzerland; 2013. last accessed Jan 29, 2018. ↩︎ ↩︎ ↩︎
TB Care I/UNAIDS. International Standards for TB care ed. Placed Published: The Hague; 2014. last accessed Jan 29, 2018. ↩︎
Huang HL, Cheng MH, Lu PL, et al. Epidemiology and Predictors of NTM Pulmonary Infection in Taiwan - a Retrospective, Five-Year Multicenter Study. Sci Rep 2017;7(1):16300. ↩︎
Griffith DE, Aksamit T, Brown-Elliott BA, et al. An official ATS/IDSA statement: diagnosis, treatment, and prevention of nontuberculous mycobacterial diseases. Am J Respir Crit Care Med 2007;175(4):367-416. ↩︎ ↩︎
Lake MA, Ambrose LR, Lipman MC, et al. '"Why me, why now?" Using clinical immunology and epidemiology to explain who gets nontuberculous mycobacterial infection. BMC Med 2016;14:54. ↩︎
Haworth CS, Banks J, Capstick T, et al. British Thoracic Society guidelines for the management of non-tuberculous mycobacterial pulmonary disease (NTM-PD). Thorax 2017;72(Suppl 2):ii1-ii64. ↩︎